13.在 100mL 0.10mol•L-1的 AgNO3(aq) 中,加入 100mL 溶有 2.08g BaCl2 的溶液,再加入 100mL 溶有 2.50g CuSO4•5H2O 的溶液,充分反应.下列说法中正确的是( )
| A. | 最终得到白色沉淀和无色溶液 | |
| B. | 最终得到的白色沉淀是等物质的量的两种化合物的混合物 | |
| C. | 混合过程中,逸出无色气体 | |
| D. | 在最终得到的溶液中,c(Cu2+)=0.01 mol•L-1 |
12.NA为阿伏伽德罗常数的值.下列叙述正确的是( )
| A. | 标准状况下,6.72L NO2与水充分反应转移的电子数目为0.2NA | |
| B. | 1mo1的Fe在1mo1Cl2中充分燃烧,转移电子数为3NA | |
| C. | 7.2g CaO2中的阴离子含有的电子数为1.0NA | |
| D. | 标准状况下,22.4L盐酸含有2NA个离子 |
8.下列说法正确的是( )
| A. | 甲烷的燃烧热为-890.3 kJ•mol-1,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3 kJ•mol-1 | |
| B. | S(g)+O2(g)═SO2(g)△H1 S(s)+O2(g)═SO2(g)△H2则△H1<△H2 | |
| C. | 已知C(石墨,s)═C(金刚石,s)△H>0,则金刚石比石墨稳定 | |
| D. | 已知中和热为△H=-57.3kJ•mol-1,则稀醋酸和稀NaOH溶液反应的热化学方程式为:CH3COOH(aq)+NaOH(aq)═CH3COONa(aq)+H2O(l)△H=-57.3 kJ•mol-1 |
7.下列说法错误的是( )
| A. | 需要加热方能发生的反应一定是吸热反应 | |
| B. | 放热的反应在常温下一定很容易发生 | |
| C. | 反应是放热还是吸热必须看反应物和生成物所具有总能量的相对大小 | |
| D. | 吸热反应在一定的条件下也能发生 |
6.下列依据热化学方程式得出的结论正确的是( )
| 热化学方程式 | 结 论 | |
| A. | 2H2(g)+O2(g)═2H2O(g)△H=-483.6 kJ/mol | 氢气的燃烧热△H=-483.6 kJ/mol |
| B. | NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l) △H=-57.3 kJ/mol | 含40.0g NaOH的稀溶液与稀醋酸完全中和,放出的热量小于57.3kJ |
| C. | 2C(s)+2O2(g)═2CO2(g)△H=-a kJ/mol 2C(s)+O2(g)═2CO(g)△H=-b kJ/mol | b>a |
| D. | C (石墨,s)═C (金刚石,s)△H=+1.5 kJ/mol | 金刚石比石墨稳定 |
| A. | A | B. | B | C. | C | D. | D |
5.由Mg、Fe、Zn组成的混合物共40g,将其放入一定量的、质量分数为25%的稀硫酸溶液中,恰好完全反应将所得溶液蒸干,共得到固体136g,用NA表示阿伏加德罗常数,则在此过程中产生氢气分子的个数为( )
| A. | lNA | B. | 2NA | C. | 3NA | D. | 0.5NA |
4.将11.9g由Mg、Al、Fe组成的合金溶于足量的NaOH溶液中,合金质量减少了2.7g.另取等质量的合金溶于过量稀硝酸中,生成了6.72L NO(标准状况下),向反应后的溶液中加入过量的NaOH溶液,则最终所得沉淀的质量为( )
0 158269 158277 158283 158287 158293 158295 158299 158305 158307 158313 158319 158323 158325 158329 158335 158337 158343 158347 158349 158353 158355 158359 158361 158363 158364 158365 158367 158368 158369 158371 158373 158377 158379 158383 158385 158389 158395 158397 158403 158407 158409 158413 158419 158425 158427 158433 158437 158439 158445 158449 158455 158463 203614
| A. | 22.1 g | B. | 27.2 g | C. | 30 g | D. | 19.4 g |

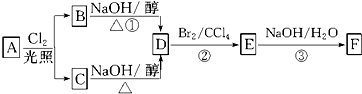
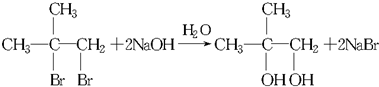 .
.