15.X酯完全燃烧生成CO2和水的物质的量之比为1:1,X经过水解得B和C,C氧化可得到B,则X酯为( )
| A. | CH3COOCH2CH2CH3 | B. | CH3CH2COOCH2CH3 | ||
| C. | CH3COOCH2CH3 | D. | CH3CH2COOCH2CH=CH2 |
14.填写下面的表格,看是否可以从这些数据中得出有用的结论:
结论:1mol任何原子的质量(以克为单位)在数值上都等于相对原子质量.
| 粒子符号 | 相对分子质量 | 每个粒子的质量(g/个) | 1mol物质含有的粒子数(个) | 1摩尔物质质量(g) |
| C | 12 | 1.993×10-23 | 6.02×1023 | |
| Fe | 56 | 9.302×10-23 | 6.02×1023 | |
| H2O | 18 | 1.628×10-22 | 6.02×1023 | |
| H2SO4 | 98 | 2.990×10-23 | 6.02×1023 | |
| Na+ | 23 | 3.821×10-23 | 6.02×1023 | |
| OH- | 17 | 2.824×10-23 | 6.02×1023 |
12.下列是某同学对相应反应的离子方程式所作的评价,其中评价合理的是( )
| 编号 | 化学反应 | 离子方程式 | 评价 |
| ① | 碳酸钙与醋酸反应 | CO32-+2CH3COOH=CO2↑+H2O+2CH3COO- | 错误,碳酸钙是弱电解质,不应写成离子形式 |
| ② | 氢氧化钠溶液中通入CO2 | OH-+CO2=HCO3- | 错误,通往过量CO2应生成CO32- |
| ③ | NaHCO3的水解 | HCO3-+H2O?H2CO3+OH- | 正确 |
| ④ | 等物质的量的FeBr2和Cl2反应 | 2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- | 正确 |
| A. | ①③ | B. | ③④ | C. | ②③ | D. | ①④ |
11.对相同状况下的12C18O和14N2两种气体,下列说法正确的是( )
| A. | 若质量相等,则质子数相等 | B. | 若原子数相等,则分子数相等 | ||
| C. | 若分子数相等,则密度相等 | D. | 若物质的量相等,则密度相等 |
9.下列叙述中,正确的是( )
| A. | 某物质只含一种元素,则该物质一定是纯净物 | |
| B. | 具有相同质子数的粒子一定属于同一种元素 | |
| C. | 任何原子都是由质子、中子和电子构成 | |
| D. | 溶液、胶体都是混合物 |
8.下列实验操作正确的是( )
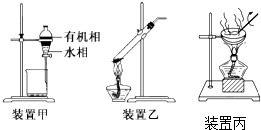

| A. | 用玻璃棒蘸取CH3COOH溶液点在水湿润的pH试纸上,测定该溶液的pH | |
| B. | 用装置甲分液,放出水相后再从分液漏斗上口放出有机相 | |
| C. | 用装置乙加热分解NaHCO3固体 | |
| D. | 用装置丙加热硫酸铜溶液获得CuSO45H2O |
7.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 1.6g由氧气和臭氧组成的混合物中含有氧原子的数目为0.1NA | |
| B. | 标准状况下,11.2L苯中含有分子的数目为0.5NA | |
| C. | 常温常压下,14g由N2与CO组成的混合气体含有的原子数目为NA | |
| D. | 物质的量浓度为1mol/L100mlHCl溶液中含0.1molHCl分子 |
6.在溶液中加入足量的Na2O2后仍能大量共存的离子组是( )
0 158258 158266 158272 158276 158282 158284 158288 158294 158296 158302 158308 158312 158314 158318 158324 158326 158332 158336 158338 158342 158344 158348 158350 158352 158353 158354 158356 158357 158358 158360 158362 158366 158368 158372 158374 158378 158384 158386 158392 158396 158398 158402 158408 158414 158416 158422 158426 158428 158434 158438 158444 158452 203614
| A. | Na+、Fe2+、Cl-、SO42- | B. | Na+、Cl-、CO32-、SO32- | ||
| C. | Ca2+、Mg2+、NO3-、HCO3- | D. | K+、AlO2-、Cl-、SO42- |