4.化学与社会、生产、生活密切相关.下列说法正确的是( )
| A. | 石英只能用于生产光导纤维 | |
| B. | 从海水中提取物质都必须通过化学反应才能实现 | |
| C. | 用SO2漂白纸浆和草帽辫 | |
| D. | 硅胶可作袋装食品的干燥剂 |
3.下列关于NO和NO2的叙述正确的是( )
| A. | NO是一种红棕色气体 | |
| B. | NO2与水反应生成硝酸,所以NO2是硝酸的酸酐 | |
| C. | NO和NO2是引发光化学烟雾的主要污染源 | |
| D. | NO2可用排水法收集 |
1.某无色溶液既可能是强酸性又可能是强碱性,在该溶液中一定能大量共存的离子是( )
| A. | H+ Na+ MnO4- SO42- | B. | Na+ CO32- Al3+ Cl- | ||
| C. | K+ Na+ Cl- SO42- | D. | K+ Cl- Ba2+ HCO3- |
20.下列说法正确的是( )
| A. | 1mol甲烷(CH4)分子中所含电子数为9NA | |
| B. | 24g镁原子的最外层电子数为NA | |
| C. | 在标准状况下,1 mol H2和1mol H2O所占的体积都约是22.4L | |
| D. | 在标准状况下,22.4L由N2和N2O组成的混合气体中,所含有的氮原子的物质的量2mol |
16.工业上一般在恒容密闭容器中采用下列反应合成甲醇:
CO(g)+2H2(g)?CH3OH(g)△H
(1)判断反应达到平衡状态的依据是(填字母序号,下同)CD.
A.生成CH3OH的速率与消耗CO的速率相等
B.混合气体的密度不变
C.混合气体的平均相对分子质量不变
D.CH3OH、CO、H2的浓度都不再发生变化
(2)如表所列数据是反应在不同温度下的化学平衡常数(K).
①由表中数据判断△H<(填“>”、“=”或“<”)0;
②某温度下,将2mol CO和6mol H2充入2L的密闭容器中,充分反应后,达到平衡时测得c(CO)=0.2mol/L,则CO的转化率为80%,此时的温度为250℃.
(3)要提高CO的转化率,可以采取的措施是DF.
A.升温 B.加入催化剂
C.增加CO的浓度 D.加入H2加压
E.加入惰性气体加压 F.分离出甲醇
(4)300℃时,在一定的压强下,5mol CO与足量的H2在催化剂的作用下恰好完全反应变化的热量为454kJ.在该温度时,在容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
下列说法正确的是D.
A.2c1>c3 B.a+b<90.8
C.2p2<p3 D.α1+α3<1.
0 158241 158249 158255 158259 158265 158267 158271 158277 158279 158285 158291 158295 158297 158301 158307 158309 158315 158319 158321 158325 158327 158331 158333 158335 158336 158337 158339 158340 158341 158343 158345 158349 158351 158355 158357 158361 158367 158369 158375 158379 158381 158385 158391 158397 158399 158405 158409 158411 158417 158421 158427 158435 203614
CO(g)+2H2(g)?CH3OH(g)△H
(1)判断反应达到平衡状态的依据是(填字母序号,下同)CD.
A.生成CH3OH的速率与消耗CO的速率相等
B.混合气体的密度不变
C.混合气体的平均相对分子质量不变
D.CH3OH、CO、H2的浓度都不再发生变化
(2)如表所列数据是反应在不同温度下的化学平衡常数(K).
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
②某温度下,将2mol CO和6mol H2充入2L的密闭容器中,充分反应后,达到平衡时测得c(CO)=0.2mol/L,则CO的转化率为80%,此时的温度为250℃.
(3)要提高CO的转化率,可以采取的措施是DF.
A.升温 B.加入催化剂
C.增加CO的浓度 D.加入H2加压
E.加入惰性气体加压 F.分离出甲醇
(4)300℃时,在一定的压强下,5mol CO与足量的H2在催化剂的作用下恰好完全反应变化的热量为454kJ.在该温度时,在容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
| 容器 | 甲 | 乙 | 丙 | |
| 反应物投入量 | 1mol CO、2mol H2 | 1mo l CH3OH | 2mol CH3OH | |
| 平衡时数据 | CH3OH的 浓度(mol/L) | c1 | c2 | c3 |
| 反应的能量变化 | a kJ | b kJ | c kJ | |
| 体系压强(Pa) | p1 | p2 | p3 | |
| 反应物转化率 | α1 | α2 | α3 | |
A.2c1>c3 B.a+b<90.8
C.2p2<p3 D.α1+α3<1.
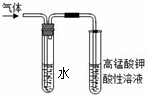 学习卤代烃的性质时,张老师通过实验的方法验证溴乙烷在不同溶剂中与NaOH 反应生成不同的反应产物,请你一起参与他们的探究.
学习卤代烃的性质时,张老师通过实验的方法验证溴乙烷在不同溶剂中与NaOH 反应生成不同的反应产物,请你一起参与他们的探究.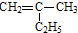 的键线式是
的键线式是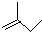
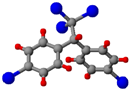 所示.请写出其结构简式
所示.请写出其结构简式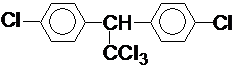
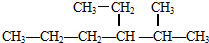 进行命名,它的名称是2-甲基-3-乙基已烷
进行命名,它的名称是2-甲基-3-乙基已烷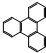 的一氯取代物有2 种.
的一氯取代物有2 种. ;Y元素在周期表中的位置是第三周期第VIA族.
;Y元素在周期表中的位置是第三周期第VIA族.