15.下列化学反应的离子方程式正确的是( )
| A. | 氢氧化镁中滴加盐酸:H++OH-═H2O | |
| B. | 碳酸氢钙溶液与稀硝酸反应:Ca(HCO3)2+2H+=Ca2++CO2↑+H2O | |
| C. | 金属铝溶于氢氧化钠溶液:2Al+6OH-═2AlO2-+3H2↑ | |
| D. | 用FeCl3溶液腐蚀铜电路板:2Fe3++Cu═2Fe2++Cu2+ |
14.同温同压下,两种气体的体积如果不相同,其主要原因是( )
| A. | 气体的分子大小不同 | B. | 气体的物质的量不同 | ||
| C. | 气体的性质不同 | D. | 气体的分子间距离不同 |
12.已知HF、CH3COOH均为弱酸,酸性强弱顺序为HF>CH3COOH,下列说法正确的是( )
| A. | 浓度均为0.1 mol•L-1的NaF、CH3COONa溶液相比较,CH3COONa溶液碱性较强 | |
| B. | 0.1 mol•L-1 CH3COOH溶液,加水稀释过程中,所有离子浓度均减小 | |
| C. | NaF溶液中只含有Na+、F-、H+、OH-、H2O五种微粒 | |
| D. | NaF溶液中加入少量NaOH固体,溶液中c(F-)变小 |
11.H+浓度相同的两份等体积溶液A和B,A为HCl溶液,B为CH3COOH溶液,二者分别和等质量的锌反应,若最后仅有一份溶液中存在锌,则下列说法正确的是( )
①开始时的反应速率:A>B ②参加反应的锌的物质的量:A=B
③反应过程的平均速率:B>A ④A中有锌剩余 ⑤B中有锌剩余.
①开始时的反应速率:A>B ②参加反应的锌的物质的量:A=B
③反应过程的平均速率:B>A ④A中有锌剩余 ⑤B中有锌剩余.
| A. | ③④ | B. | ③⑤ | C. | ①③④ | D. | ①②③ |
10.下列烷烃的一氯取代物中没有同分异构体的是( )
| A. | 2-甲基丙烷 | B. | 丙烷 | C. | 丁烷 | D. | 甲烷 |
9.(1)25℃时,部分物质的电离平衡常数如表所示:
CH3COOH、H2CO3、HClO的酸性由强到弱的顺序CH3COOH>H2CO3>HClO.
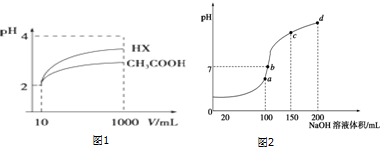
(2)体积为10mL pH=2的醋酸溶液与一元酸HX溶液分别加水稀释至1000mL,稀释过程pH变化如图1:则HX的电离平衡常数大于(填“大于”、“等于”或“小于”)醋酸的平衡常数.
(3)H+浓度相同等体积的两份溶液A(盐酸)和B(CH3COOH)分别与锌粉反应,若最后仅有一份溶液中存在锌,放出氢气的质量相同,则下列说法正确的是③④⑤ (填写序号).
①反应所需要的时间B>A ②开始反应时的速率A>B
③参加反应的锌的物质的量A=B ④反应过程的平均速率B>A
⑤A 中有锌剩余 ⑥B中有锌剩余
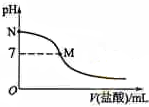
(4)室温时,向100mL 0.1mol•L-1NH4HSO4溶液中滴加0.1mol•L-1NaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图2所示:试分析图中a、b、c、d四个点,水的电离程度最大的是a;在b点,溶液
中各离子浓度由大到小的排列顺序是c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+).
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | 1.7×10-5 | K1=4.3×10-7 K2=5.6×10-11 | 3.0×10-8 |
(2)体积为10mL pH=2的醋酸溶液与一元酸HX溶液分别加水稀释至1000mL,稀释过程pH变化如图1:则HX的电离平衡常数大于(填“大于”、“等于”或“小于”)醋酸的平衡常数.

(3)H+浓度相同等体积的两份溶液A(盐酸)和B(CH3COOH)分别与锌粉反应,若最后仅有一份溶液中存在锌,放出氢气的质量相同,则下列说法正确的是③④⑤ (填写序号).
①反应所需要的时间B>A ②开始反应时的速率A>B
③参加反应的锌的物质的量A=B ④反应过程的平均速率B>A
⑤A 中有锌剩余 ⑥B中有锌剩余
(4)室温时,向100mL 0.1mol•L-1NH4HSO4溶液中滴加0.1mol•L-1NaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图2所示:试分析图中a、b、c、d四个点,水的电离程度最大的是a;在b点,溶液
中各离子浓度由大到小的排列顺序是c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+).
8. 298K时,在20.0mL 0.10mol•L-1氨水中滴入0.10mol•L-的盐酸,溶液的pH与所加盐酸的体积关系如图所示.已知0.10mol•L-1氨水的电离度为1.32%,下列有关叙述正确的是( )
298K时,在20.0mL 0.10mol•L-1氨水中滴入0.10mol•L-的盐酸,溶液的pH与所加盐酸的体积关系如图所示.已知0.10mol•L-1氨水的电离度为1.32%,下列有关叙述正确的是( )
 298K时,在20.0mL 0.10mol•L-1氨水中滴入0.10mol•L-的盐酸,溶液的pH与所加盐酸的体积关系如图所示.已知0.10mol•L-1氨水的电离度为1.32%,下列有关叙述正确的是( )
298K时,在20.0mL 0.10mol•L-1氨水中滴入0.10mol•L-的盐酸,溶液的pH与所加盐酸的体积关系如图所示.已知0.10mol•L-1氨水的电离度为1.32%,下列有关叙述正确的是( )| A. | 该滴定过程应该选择石蕊作为指示剂 | |
| B. | M点对应的盐酸体积为20.0 mL | |
| C. | M点处的溶液中c(NH4+)=c(Cl-)=c(H+)=c(OH-) | |
| D. | N点处的溶液中pH<12 |
7.过氧乙酸(CH3COOOH)有强氧化性,用于物体表面、皮肤、果蔬、环境的消毒,其制备反应为:CH3COOH+H2O2?CH3COOOH+H2O,下列有关说法正确的是( )
| A. | 降低温度可加快该反应速率 | |
| B. | 加入合适的催化剂可提高H2O2转化率 | |
| C. | 达到平衡时,v(正)=v(逆)=0 | |
| D. | 达到平衡时,v正(CH3COOH)=v逆(H2O2) |
6.已知aAn+、bB(n+1)+、cCn-、dD(n+1)-均是具有相同电子层结构的短周期元素形成的简单离子,下列说法正确的是( )
0 158224 158232 158238 158242 158248 158250 158254 158260 158262 158268 158274 158278 158280 158284 158290 158292 158298 158302 158304 158308 158310 158314 158316 158318 158319 158320 158322 158323 158324 158326 158328 158332 158334 158338 158340 158344 158350 158352 158358 158362 158364 158368 158374 158380 158382 158388 158392 158394 158400 158404 158410 158418 203614
| A. | 原子半径C>D>A>B | B. | 离子半径D>C>B>A | ||
| C. | 原子序数b>a>c>d | D. | 单质的还原性A>B>C>D |