5.①某环保监测站对刚降下的雨水定时测定其pH,数据如表:
请写出酸雨形成过程中所涉及反应的化学方程式SO2+H2O?H2SO3,2H2SO3+O2═2H2SO4.
②我国是燃煤大国,若某家庭取暖每天燃烧 6.4kg 煤,煤中硫元素的质量分数为 1%.假设煤中的硫全部转化为 SO2,试计算每天产生的 SO2的体积(标准状况下).
③治理燃煤大都采用的是石灰石-石膏法脱硫,试写出脱硫过程中发生反应的主要化学方程式,CaCO3+SO2$\frac{\underline{\;高温\;}}{\;}$CaSO3+CO2,2CaSO3+O2$\frac{\underline{\;高温\;}}{\;}$2CaSO4.
| 测定时间/min | 0 | 1 | 2 | 4 | 5 |
| pH | 4.73 | 4.62 | 4.56 | 4.55 | 4.55 |
②我国是燃煤大国,若某家庭取暖每天燃烧 6.4kg 煤,煤中硫元素的质量分数为 1%.假设煤中的硫全部转化为 SO2,试计算每天产生的 SO2的体积(标准状况下).
③治理燃煤大都采用的是石灰石-石膏法脱硫,试写出脱硫过程中发生反应的主要化学方程式,CaCO3+SO2$\frac{\underline{\;高温\;}}{\;}$CaSO3+CO2,2CaSO3+O2$\frac{\underline{\;高温\;}}{\;}$2CaSO4.
3.下列说法不正确的是( )
| A. | 光导纤维的主要成分是 SiO2 | |
| B. | 石英玻璃常用来制耐高温的化学仪器 | |
| C. | 硅酸盐工业使用的每一种原料中都含有硅 | |
| D. | 水泥和普通玻璃都是混合物 |
2.香烟燃烧产生的烟气中有多种有害物质,其中尼古丁(C10H14N2)对人体危害 大,下列关于尼古丁的说法正确的是( )
| A. | 是由26个原子构成的物质 | B. | 氮元素的质量分数为17.3% | ||
| C. | C、H、O 元素的质量比为10:14:2 | D. | 相对分子质量是162g |
20.下列说法中,正确的是( )
| A. | 在纯水中加入硫酸或醋酸钠都会抑制水的电离 | |
| B. | 常温下,0.lmo1•Lˉ1氯化铵溶液加水稀释,溶液中的c(OHˉ)增大 | |
| C. | 1mL pH=2的醋酸溶液加水稀释到l0mL,pH变为3 | |
| D. | 常温下,0.1mol•L?1氨水加水稀释,溶液中的c(OHˉ)增大 |
17.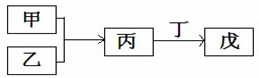 甲、乙、丙、丁、戊是中学常见的无机物,其中甲、乙为单质,它们的转化关系如图所示(某些条件和部分产物已略去).下列说法不正确的是( )
甲、乙、丙、丁、戊是中学常见的无机物,其中甲、乙为单质,它们的转化关系如图所示(某些条件和部分产物已略去).下列说法不正确的是( )
 甲、乙、丙、丁、戊是中学常见的无机物,其中甲、乙为单质,它们的转化关系如图所示(某些条件和部分产物已略去).下列说法不正确的是( )
甲、乙、丙、丁、戊是中学常见的无机物,其中甲、乙为单质,它们的转化关系如图所示(某些条件和部分产物已略去).下列说法不正确的是( )| A. | 若甲、丙、戊含有同一种元素,则三种物质中,该元素的化合价由低到高的顺序一定为:甲<丙<戊 | |
| B. | 若甲为短周期中原子半径最大的主族元素的单质,且戊为碱,则丙可能为Na2O2 | |
| C. | 若丙、丁混合产生白烟,且丙分子为18电子分子,丁分子为10电子分子,则乙的水溶液可能具有漂白作用 | |
| D. | 若甲既能与盐酸反应又能与NaOH溶液反应,则丙可能属于两性氧化物 |
16.下列依据相关实验得出的结论正确的是( )
0 158219 158227 158233 158237 158243 158245 158249 158255 158257 158263 158269 158273 158275 158279 158285 158287 158293 158297 158299 158303 158305 158309 158311 158313 158314 158315 158317 158318 158319 158321 158323 158327 158329 158333 158335 158339 158345 158347 158353 158357 158359 158363 158369 158375 158377 158383 158387 158389 158395 158399 158405 158413 203614
| A. | 用铂丝蘸取少量某溶液进行焰色反应,透过蓝色钴玻璃观察到火焰呈紫色,该溶液一定是钾盐溶液 | |
| B. | 在0.1mol•L-1Na2CO3溶液中,加两滴酚酞显浅红色,微热后红色加深,说明盐类水解反应是吸热反应 | |
| C. | 向某FeCl2 溶液中加入KSCN溶液,观察到溶液呈血红色,说明该溶液中FeCl2已全部被氧化 | |
| D. | 向某溶液中加入稀盐酸,产生的气体通入澄清石灰水,石灰水变浑浊,该溶液一定含有CO32- |
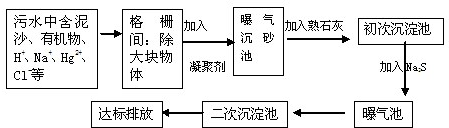
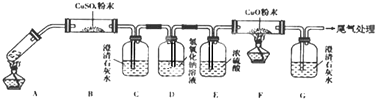
 如图所示,甲、乙两池的电极材料都是铁棒与碳棒,
如图所示,甲、乙两池的电极材料都是铁棒与碳棒,