15.下列说法正确的是( )
| A. | 在多电子的原子里,能量高的电子通常在离核近的区域内活动 | |
| B. | 任何元素的原子都是由核外电子和核内中子、质子组成的 | |
| C. | 核素指一种原子,而元素是指一类原子;核素间互称同位素,元素包含同位素 | |
| D. | ${\;}_{18}^{40}$Ar、${\;}_{19}^{40}$K、${\;}_{20}^{40}$Ca的质量数相同,所以它们是互为同位素 |
12.下列各组离子能大量共存于同一溶液中,且加入少量NaOH溶液或少量稀硫酸时都能产生白色沉淀的是( )
| A. | Ba2+、Mg2+、NO3-、CO32- | B. | Na+、Ag+、Cl-、Ba2+ | ||
| C. | K+、Ba2+、Cl-、HCO3- | D. | Ba2+、Na+、NO3-、Cl- |
11.25℃时,10mL 0.1mol•L-1 的一元酸HA溶液,在水中约有0.1%发生电离(每1000个HA只有1个HA电离),下列叙述不正确的是( )
| A. | 该溶液的pH约是4 | |
| B. | HA一定是一种弱酸 | |
| C. | 恰好中和时消耗NaOH的物质的量是10-6mol | |
| D. | 与足量Mg完全反应生成标准状况下气体的体积可能是11.2 mL |
10.一定条件下的反应N2(g)+3H2(g)?2NH3(g)达到化学平衡的本质原因是( )
| A. | 正、逆反应的速率相等且不为0 | B. | 反应体系中的气体压强保持不变 | ||
| C. | 正、逆反应都还在继续进行 | D. | 反应混合物中各组分的浓度相等 |
8.下列反应的离子方程式书写正确的是( )
| A. | 钠和冷水反应:Na+2H2O═Na++2OH-?+H2↑ | |
| B. | 金属铝溶于氢氧化钠溶液:Al+2OH-═AlO2-?+H2↑ | |
| C. | 铁跟稀硫酸反应:2Fe+6H+═2Fe3++3H2↑ | |
| D. | FeCl2溶液跟Cl2反应:2Fe2++Cl2═2Fe3++2Cl- |
7.水的电离平衡曲线如图所示,下列说法不正确的是( )
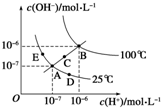

| A. | 图中五点Kw的关系:B>C>A=D=E | |
| B. | 若从A 点到D 点,可采用:温度不变向水中加入少量的酸 | |
| C. | 若从A 点到C 点,可采用:温度不变向水中加入适量的NH4Cl 固体 | |
| D. | 若处在B 点时,将pH=2 的硫酸与pH=10 的KOH 溶液等体积混合后,溶液显中性 |
6.用下列实验装置或操作进行的实验能达到实验目的是( )
0 158200 158208 158214 158218 158224 158226 158230 158236 158238 158244 158250 158254 158256 158260 158266 158268 158274 158278 158280 158284 158286 158290 158292 158294 158295 158296 158298 158299 158300 158302 158304 158308 158310 158314 158316 158320 158326 158328 158334 158338 158340 158344 158350 158356 158358 158364 158368 158370 158376 158380 158386 158394 203614
| A. | 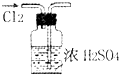 干燥Cl2 | B. | 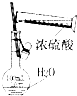 配制100ml 0.1mol•L-1硫酸溶液 | ||
| C. | 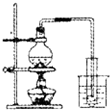 制取少量蒸馏水 | D. |  检验钾元素的存在 |
 A、B、C、D四种短周期元素,原子序数D>A>B>C,且A、B、D同周期,C、D同主族,A的原子结构示意图如图,B、C可形成离子化合物B2C2或B2C据此填空:
A、B、C、D四种短周期元素,原子序数D>A>B>C,且A、B、D同周期,C、D同主族,A的原子结构示意图如图,B、C可形成离子化合物B2C2或B2C据此填空: