13.下列4个有机化合物中,能够发生酯化、加成和氧化3种反应的是( )
①CH2=CHCOOH ②CH2=CHCOOCH3 ③CH3CH2CH2OH ④CH2=CHCH2OH⑤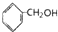
①CH2=CHCOOH ②CH2=CHCOOCH3 ③CH3CH2CH2OH ④CH2=CHCH2OH⑤

| A. | ①③ | B. | ①④⑤ | C. | ②④ | D. | ①②③⑤ |
12.下列变化不能用勒夏特列原理解释的是( )
| A. | 工业生产硫酸的过程中使用过量的空气,以提高二氧化硫的转化率 | |
| B. | 氯化镁溶液加热蒸干最终得不到氯化镁固体 | |
| C. | 合成氨是放热反应,采用在较高温度下进行反应 | |
| D. | 实验室用排饱和食盐水的方法收集氯气 |
11.对于反应A(g)+3B(g)?2C(s)+D(g),用下列各数据表示不同条件下的反应速度,其中反应进行得最快的是( )
| A. | v(A)=0.01mol•L-1s-1 | B. | v(B)=0.02mol•L-1s-1 | ||
| C. | v(C)=1.50mol•L-1min-1 | D. | v(D)=0.50mol•L-1min-1 |
10.下面的排序正确的是( )
| A. | 晶体熔点由低到高:CCl4<CBr4<CI4<CF4 | |
| B. | 晶格能由大到小:NaF>NaCl>NaBr>NaI | |
| C. | 熔点由高到低:Na>Mg>Al | |
| D. | 硬度由大到小:金刚石>晶体硅>碳化硅 |
9.下列现象与氢键有关的是( )
①NH3的熔、沸点比VA族其他元素氢化物的熔、沸点高
②小分子的醇、羧酸可以和水以任意比互溶
③邻羟基苯甲酸的熔、沸点比对羟基苯甲酸的熔、沸点低
④水分子高温下也很稳定
⑤水分子较硫化氢分子稳定.
①NH3的熔、沸点比VA族其他元素氢化物的熔、沸点高
②小分子的醇、羧酸可以和水以任意比互溶
③邻羟基苯甲酸的熔、沸点比对羟基苯甲酸的熔、沸点低
④水分子高温下也很稳定
⑤水分子较硫化氢分子稳定.
| A. | ①②③ | B. | ④⑤ | C. | ③④⑤ | D. | ①②③④ |
7.一个化学反应,我们不但要关心物质变化,还要研究外界条件对化学反应速率和反应限度的影响.
(Ⅰ)某学生为了探究锌与盐酸反应生成氢气过程中的速率变化,他在100mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
(1)哪一时间段反应速率最大2~3min,原因是反应放热,加快反应速率.(指0~1、1~2、2~3、3~4、4~5min)
(2)哪一段时段的反应速率最小4~5min,原因是盐酸浓度减小(氢离子浓度减小).
(3)如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,可在盐酸中分别加入等体积的下列溶液,你认为可行的是B.
A.Na2CO3溶液 B.NaCl溶液 C.NaNO3溶液 D.CuSO4溶液
(Ⅱ)一定温度下,将3molA气体和1mol B气体通入一容积固定为2L的密闭容器中,发生如下反应:3A(g)+B(g)?xC(g),反应1min时测得剩余1.8molA,C的浓度为0.4mol/L,则1min内,B的平均反应速率为0.2mol/(L.min);X为2.若反应经2min达到平衡,平衡时C的浓度小于0.8mol/L(填“大于”,“小于”或“等于”).若已知达平衡时,该容器内混合气体总压强为p,混合气体起始压强为p0.请用p0、p来表示达平衡时反应物A的转化率为$\frac{2{P}_{0}-2P}{{P}_{0}}$×100%.
提示:$物质的转化率(%)=\frac{反应物转化的物质的量}{反应物起始的物质的量}×100%$.
(Ⅰ)某学生为了探究锌与盐酸反应生成氢气过程中的速率变化,他在100mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL) | 50 | 120 | 232 | 290 | 310 |
(2)哪一段时段的反应速率最小4~5min,原因是盐酸浓度减小(氢离子浓度减小).
(3)如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,可在盐酸中分别加入等体积的下列溶液,你认为可行的是B.
A.Na2CO3溶液 B.NaCl溶液 C.NaNO3溶液 D.CuSO4溶液
(Ⅱ)一定温度下,将3molA气体和1mol B气体通入一容积固定为2L的密闭容器中,发生如下反应:3A(g)+B(g)?xC(g),反应1min时测得剩余1.8molA,C的浓度为0.4mol/L,则1min内,B的平均反应速率为0.2mol/(L.min);X为2.若反应经2min达到平衡,平衡时C的浓度小于0.8mol/L(填“大于”,“小于”或“等于”).若已知达平衡时,该容器内混合气体总压强为p,混合气体起始压强为p0.请用p0、p来表示达平衡时反应物A的转化率为$\frac{2{P}_{0}-2P}{{P}_{0}}$×100%.
提示:$物质的转化率(%)=\frac{反应物转化的物质的量}{反应物起始的物质的量}×100%$.
6.下列装置能组成原电池的是( )
| A. | 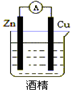 | B. | 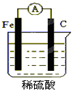 | C. | 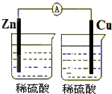 | D. | 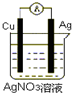 |
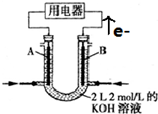
4.微型纽扣电池在现代生活中是广泛应用的一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH溶液,电池总反应式为Ag2O+Zn═2Ag+ZnO.根据上述反应式,判断下列叙述中正确的是( )
0 158183 158191 158197 158201 158207 158209 158213 158219 158221 158227 158233 158237 158239 158243 158249 158251 158257 158261 158263 158267 158269 158273 158275 158277 158278 158279 158281 158282 158283 158285 158287 158291 158293 158297 158299 158303 158309 158311 158317 158321 158323 158327 158333 158339 158341 158347 158351 158353 158359 158363 158369 158377 203614
| A. | 在使用过程中,电池负极区溶液pH增大 | |
| B. | 在使用过程中,电子由Ag2O极经外电路流向Zn极 | |
| C. | 在使用过程中,Zn电极发生还原反应,Ag2O电极发生氧化反应 | |
| D. | 外电路中每通过0.2 mol电子,正极的质量理论上减小1.6 g |
 在化学反应中,反应物转化成生成物,必然发生能量的变化.
在化学反应中,反应物转化成生成物,必然发生能量的变化.