12.下列叙述中,正确的是( )
| A. | 两种粒子,若核外电子排布完全相同,则其化学性质一定完全相同 | |
| B. | 凡单原子形成的离子,一定具有稀有气体元素原子的核外电子排布 | |
| C. | 两原子如果核外电子排布相同,则一定具有相同的中子数 | |
| D. | 某离子M层和L层上的电子均为K层的4倍 |
11.某烃相对分子质量为82,试判断它可能是( )
| A. | 环烷烃 | B. | 芳香烃 | ||
| C. | 含有5个碳原子的烃 | D. | 二烯烃 |
9.常温下,向25mL 0.1mol•L-1弱碱MOH溶液中逐滴滴加0.2mol•L-1的HCl,溶液pH的变化曲线如图所示(溶液混合时体积的变化忽略不计).下列说法正确的是( )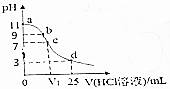

| A. | MOH电离方程式为:MOH═M++OH- | |
| B. | 在b点,离子浓度大小为c(OH-)>c(H+)>c(M+)>c(Cl-) | |
| C. | 在c点,滴加的V(HCl)>12.5mL | |
| D. | 在d点,c(Cl-)=2c(MOH)+2c(M+)=0.1mol•L-1 |
6.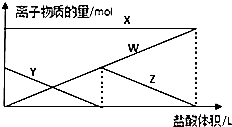 向aL1mol•L-1的Na2CO3的溶液中缓慢地滴加bL1mol•L-1的盐酸,并不断搅拌,随着盐酸的加入,溶液中离子物质的量也相应地发生变化如图所示(不考虑盐类的水解及水的电离),下列说法正确的是( )
向aL1mol•L-1的Na2CO3的溶液中缓慢地滴加bL1mol•L-1的盐酸,并不断搅拌,随着盐酸的加入,溶液中离子物质的量也相应地发生变化如图所示(不考虑盐类的水解及水的电离),下列说法正确的是( )
 向aL1mol•L-1的Na2CO3的溶液中缓慢地滴加bL1mol•L-1的盐酸,并不断搅拌,随着盐酸的加入,溶液中离子物质的量也相应地发生变化如图所示(不考虑盐类的水解及水的电离),下列说法正确的是( )
向aL1mol•L-1的Na2CO3的溶液中缓慢地滴加bL1mol•L-1的盐酸,并不断搅拌,随着盐酸的加入,溶液中离子物质的量也相应地发生变化如图所示(不考虑盐类的水解及水的电离),下列说法正确的是( )| A. | 四条线与溶液中离子的对应关系是:X:Na+;Y:CO32-;Z:Cl-;W:HCO3- | |
| B. | 当a<b<2a时,发生的离子方程式为:CO32-+H+=CO2↑+H2O | |
| C. | 当3b=2a时,发生的离子方程式为:HCO3-+H+=CO2↑+H2O | |
| D. | 当$\frac{a}{2}$<b<a时,溶液中HCO32-与CO32-的物质的量之比为b:(a-b) |
4.已知:2NaAlO2+CO2+3H2O=2A1(OH)3↓+Na2CO3,向含2molNaOH、1molBa(OH)2、2molNaAlO2的混合溶液中慢慢通人CO2,则通人CO2的量和生成沉淀的量的关系正确的是( )
| 选项 | A | B | C | D |
| n(CO2)/mol | 2 | 3 | 4 | 5 |
| n(沉淀)/mol | 2 | 2 | 3 | 2 |
| A. | A | B. | B | C. | C | D. | D |
3.有3种溶液①0.01mol•L-1醋酸; ②0.02mol•L-1醋酸与0.02mol•L-1NaOH等体积混合后的溶液;③0.04mol•L-1醋酸与0.02mol•L-1 NaOH等体积混合后的溶液.下列说法不正确的是( )
0 158173 158181 158187 158191 158197 158199 158203 158209 158211 158217 158223 158227 158229 158233 158239 158241 158247 158251 158253 158257 158259 158263 158265 158267 158268 158269 158271 158272 158273 158275 158277 158281 158283 158287 158289 158293 158299 158301 158307 158311 158313 158317 158323 158329 158331 158337 158341 158343 158349 158353 158359 158367 203614
| A. | 相同温度下,溶液中水的电离程度:溶液①<溶液② | |
| B. | 可用Na2CO3固体鉴别0.04mol•L-1醋酸和0.04mol•L-1盐酸 | |
| C. | 向①中加入少量CH3COONa固体,则$\frac{{K}_{a}}{c(C{H}_{3}CO{O}^{-})}$增大 | |
| D. | 加水稀释溶液③,溶液中$\frac{c(C{H}_{3}COOH)•c(O{H}^{-})}{c(C{H}_{3}CO{O}^{-})}$不变 |
 用0.1000mol•L-1NaOH溶液滴定20.00mL某未知浓度的醋酸溶液,滴定曲线如图所示.其中①点所示溶液中c(CH3COO-)=2c(CH3COOH),则CH3COOH的电离平衡常数Ka=2×10-5mol/L.
用0.1000mol•L-1NaOH溶液滴定20.00mL某未知浓度的醋酸溶液,滴定曲线如图所示.其中①点所示溶液中c(CH3COO-)=2c(CH3COOH),则CH3COOH的电离平衡常数Ka=2×10-5mol/L.