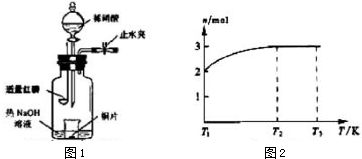
2.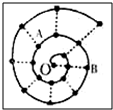 某同学在研究前18号元素时发现,可以将它们排成如图所示的“蜗牛”形状,图中每个弧线上的“•”代表一种元素,其中O点代表氢元素.下列说法中正确的是( )
某同学在研究前18号元素时发现,可以将它们排成如图所示的“蜗牛”形状,图中每个弧线上的“•”代表一种元素,其中O点代表氢元素.下列说法中正确的是( )
 某同学在研究前18号元素时发现,可以将它们排成如图所示的“蜗牛”形状,图中每个弧线上的“•”代表一种元素,其中O点代表氢元素.下列说法中正确的是( )
某同学在研究前18号元素时发现,可以将它们排成如图所示的“蜗牛”形状,图中每个弧线上的“•”代表一种元素,其中O点代表氢元素.下列说法中正确的是( )| A. | 离O点越远的元素越容易失去电子 | |
| B. | 虚线相连的元素处于同一周期 | |
| C. | B元素是图中原子半径最大的主族元素 | |
| D. | 元素O和A可形成多种化合物、和B不能形成化合物 |
19.用惰性电极电解下列溶液,一段时间(时间较短)后,再加入一定质量的另一种物质(小括号内),溶液能与原来溶液完全一样的是( )
| A. | CuCl2(无水CuSO4) | B. | NaOH(H2O) | C. | NaCl(HCl气体) | D. | CuSO4(Cu(OH)2固体) |
18.可逆反应N2(g)+3H2(g)?2NH3(g)△H<0,在达到平衡时,要使NH3的浓度达到最大值,最适宜的条件是( )
| A. | 低温高压 | B. | 低温低压 | C. | 高温高压 | D. | 使用合适催化剂 |
17.常温下,0.1mol/L氨水溶液中$\frac{c({H}^{+})}{c(O{H}^{-})}$=1×10-8,下列叙述不正确的是( )
| A. | 该溶液中氢离子的浓度:c(H+)=1×10-11 mol/L | |
| B. | 0.1 mol/L氨水溶液与0.1 mol/L HCl溶液等体积混合后所得溶液中:c(NH4+)+c(H+)=c(Cl-)+c(OH-) | |
| C. | 0.1 mol/L的氨水溶液与0.05 mol/L H2SO4溶液等体积混合后所得溶液中:c(NH4+)+c(NH3•H2O)=2c(SO42-) | |
| D. | 浓度均为0.1 mol/L的NH3•H2O和NH4Cl溶液等体积混合后,若溶液呈碱性,则c(NH4+)>c(NH3•H2O)>c(Cl-)>c(OH-)>c(H+) |
13.迄今为止合成的最重的元素是112号元素,它是用${\;}_{30}^{70}$Zn高能原子轰击${\;}_{82}^{208}$Pb的靶子,使锌核与铅核熔合而得,每生成一个112号元素的原子(${\;}_{112}^{277}$R)的同时向外释放出一个中子.下列说法错误的是( )
0 158156 158164 158170 158174 158180 158182 158186 158192 158194 158200 158206 158210 158212 158216 158222 158224 158230 158234 158236 158240 158242 158246 158248 158250 158251 158252 158254 158255 158256 158258 158260 158264 158266 158270 158272 158276 158282 158284 158290 158294 158296 158300 158306 158312 158314 158320 158324 158326 158332 158336 158342 158350 203614
| A. | 112号元素是金属元素 | |
| B. | 112号元素位于第七周期,是主族元素 | |
| C. | ${\;}_{112}^{277}$R原子中子数为165 | |
| D. | 112号元素为放射性元素 |
 ;
; .
.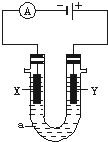 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:

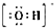 .
.