8.1g氢气完全燃烧生成液态水放出142.9kJ的热量,表示该反应的热化学方程式为( )
| A. | 2H2+O2→2H2O+571.6 kJ | B. | 2H2(g)+O2(g)→2H2O(1)+142.9 kJ | ||
| C. | 2H2O(g)+O2(g)→2H2O(g)+571.6 kJ | D. | H2(g)+$\frac{1}{2}$O2(g)→H2O(1)+285.8 kJ |
7.下列溶液一定呈中性的是( )
| A. | c(H+)=1×10-7 mol/L | B. | c(OH-)=1×10-7mol/L | ||
| C. | c(H+)=c(OH-) | D. | pH=7 |
6.已知充分燃烧a g乙炔气体时生成1mol二氧化碳气体和液态水,并放出热量b kJ,则乙炔燃烧的热化学方程式正确的是( )
| A. | 2C2H2(g)+5O2(g) 4CO2(g)+2H2O(l);△H=-4b kJ/mol | |
| B. | C2H2(g)+$\frac{5}{2}$O2(g) 2CO2(g)+H2O(l);△H=2b kJ/mol | |
| C. | 2C2H2(g)+5O2(g) 4CO2(g)+2H2O(l);△H=-2b kJ/mol | |
| D. | 2C2H2(g)+5O2(g) 4CO2(g)+2H2O(l);△H=b kJ/mol |
5.19世纪中叶,俄国化学家门捷列夫的突出贡献是( )
| A. | 得出完整的元素周期表 | B. | 发现了元素周期律 | ||
| C. | 发现空气的组成 | D. | 提出原子、分子学说 |
4.在直流电的作用下,锌板上镀铜时,金属铜作( )
| A. | 阳极 | B. | 阴极 | C. | 正极 | D. | 负极 |
3.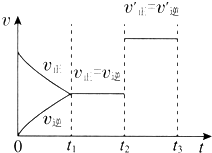 如图表示一定条件下N2+3H2?2NH3的反应速率和时间的关系,其中t1是达到平衡需要的时间,t2~t3是改变一个条件后出现的情况,则该条件可能是( )
如图表示一定条件下N2+3H2?2NH3的反应速率和时间的关系,其中t1是达到平衡需要的时间,t2~t3是改变一个条件后出现的情况,则该条件可能是( )
0 158135 158143 158149 158153 158159 158161 158165 158171 158173 158179 158185 158189 158191 158195 158201 158203 158209 158213 158215 158219 158221 158225 158227 158229 158230 158231 158233 158234 158235 158237 158239 158243 158245 158249 158251 158255 158261 158263 158269 158273 158275 158279 158285 158291 158293 158299 158303 158305 158311 158315 158321 158329 203614
 如图表示一定条件下N2+3H2?2NH3的反应速率和时间的关系,其中t1是达到平衡需要的时间,t2~t3是改变一个条件后出现的情况,则该条件可能是( )
如图表示一定条件下N2+3H2?2NH3的反应速率和时间的关系,其中t1是达到平衡需要的时间,t2~t3是改变一个条件后出现的情况,则该条件可能是( )| A. | 加压 | B. | 升温 | C. | 加入催化剂 | D. | 增大反应物浓度 |
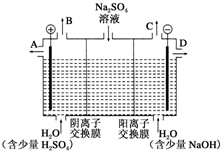 芒硝化学式为Na2SO4•10H2O,无色晶体,易溶于水,是一种分布很广泛的硫酸盐矿物.该小组同学设想,如果模拟工业上离子交换膜法制烧碱的方法,用如图所示装置电解硫酸钠溶液来制取氢气、氧气、硫酸和氢氧化钠,无论从节省能源还是从提高原料的利用率而言都更加符合绿色化学理念.
芒硝化学式为Na2SO4•10H2O,无色晶体,易溶于水,是一种分布很广泛的硫酸盐矿物.该小组同学设想,如果模拟工业上离子交换膜法制烧碱的方法,用如图所示装置电解硫酸钠溶液来制取氢气、氧气、硫酸和氢氧化钠,无论从节省能源还是从提高原料的利用率而言都更加符合绿色化学理念.
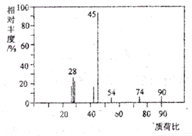 有机物A常用于食品行业.已知9.0gA在足量O2中充分燃烧,混合气体依次通过足量的浓硫酸和碱石灰,分别增重5.4g和13.2g,经检验剩余气体为O2.
有机物A常用于食品行业.已知9.0gA在足量O2中充分燃烧,混合气体依次通过足量的浓硫酸和碱石灰,分别增重5.4g和13.2g,经检验剩余气体为O2. I氮是地球上极为丰富的元素,氮及其化合物与人们的生活息息相关.在氮的单质和常见化合物中:
I氮是地球上极为丰富的元素,氮及其化合物与人们的生活息息相关.在氮的单质和常见化合物中: .
.