11.下列关于热化学反应的描述中正确的是( )
| A. | CO(g)的燃烧热是283.0kJ/mol,则2CO2(g)=2CO(g)+O2(g)反应的△H=+2×283.0kJ/mol | |
| B. | HCl和NaOH反应的中和热△H=-57.3kJ/mol,则H2SO4和Ba(OH)2反应的中和热△H=2×(-57.3)kJ/mol | |
| C. | 需要加热才能发生的反应一定是吸热反应 | |
| D. | 已知反应H2S(g)+a O2(g)═X+c H2O(l)△H,若△H表示该反应的燃烧热,则X为SO2(g) |
10.下列说法正确的是( )
| A. | 等物质的量的硫固体和硫蒸气分别完全燃烧,后者放出的热量多 | |
| B. | 植物通过光合作用将二氧化碳转化为葡萄糖是太阳能转化为热能的过程 | |
| C. | 在101kPa时,1mol纯物质完全燃烧时所放出的热量叫做该物质的燃烧热 | |
| D. | 热化学方程式中的△H的值与反应物的用量有关 |
6.实验室制取高锰酸钾必须用锰酸钾(K2MnO4)配成电解质溶液,以铁、石墨分别作电极进行电解.有关此制备实验的下列叙述中,正确的是( )
| A. | 石墨为阴极,阳极上有气体产生 | |
| B. | 铁作阳极,阴极的反应式为2H++2e-═H2 | |
| C. | 铁作阴极,阳极的反应式为2 MnO42--2e-═2 MnO4- | |
| D. | 石墨为阳极,阴极的反应式为2 MnO42--2e-═2 MnO4- |
4.与自然界中的许多变化一样,化学反应具有方向性.下列有关叙述中正确的是( )
| A. | 原电池反应一定是自发进行的氧化还原反应,且△H<0 | |
| B. | △H<0,△S<0的反应肯定能自发进行 | |
| C. | 体系能量增大和混乱度增大都有促使反应自发进行的倾向 | |
| D. | CaCO3(s)=CaO(s)+CO2(g)的△H>0,△S<0,该反应在较高温度下能自发进行 |
3.在l01kPa时燃烧1t含FeS2质量分数为70%的黄铁矿(杂质不参加反应)生成固态Fe2O3和气 态SO2,放出4.98×106kJ的热量.表示上述反应的热化学方程式正确的是( )
0 158133 158141 158147 158151 158157 158159 158163 158169 158171 158177 158183 158187 158189 158193 158199 158201 158207 158211 158213 158217 158219 158223 158225 158227 158228 158229 158231 158232 158233 158235 158237 158241 158243 158247 158249 158253 158259 158261 158267 158271 158273 158277 158283 158289 158291 158297 158301 158303 158309 158313 158319 158327 203614
| A. | 4FeS2( s)+11O2( g)═2Fe2O3( s)+8SO2(g)△H=-3414.8kJ•moL | |
| B. | FeS2(s)+$\frac{11}{4}$O2(g)═$\frac{1}{2}$Fe2O3 (s)+2SO2(g)△H=-853.7kJ•moL | |
| C. | 4FeS2(s)+11O2(g)═2 Fe2O3 (s)+8SO2(g)△H+3414.8kJ•moL | |
| D. | FeS2(s)+$\frac{11}{4}$O2(g)═$\frac{1}{2}$Fe2O3 (s)+2SO2(g)△H=+853.7kJ•moL |
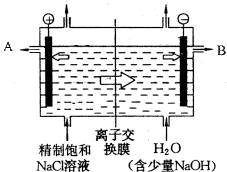 工业上电解制烧碱的技术是用离子交换膜法,主要原料是饱和食盐水.图为离子交换膜法电解原理示意图:
工业上电解制烧碱的技术是用离子交换膜法,主要原料是饱和食盐水.图为离子交换膜法电解原理示意图: