3.萤火虫的发光是荧光素在催化作用下发生复杂的生化反应并释放光能,其原理可以简单表示如下:

关于荧光素及氧化荧光素的叙述,正确的是( )

关于荧光素及氧化荧光素的叙述,正确的是( )
| A. | 互为同系物 | B. | 均可发生硝化反应 | ||
| C. | 均可与碳酸氢钠反应 | D. | 均最多有7个碳原子共平面 |
2.下列关于有机物的说法中,不正确的是( )
| A. | 液化石油气和天然气的主要成分都是甲院 | |
| B. | 苯、乙醇和乙酸都能发生取代反应 | |
| C. | 油脂在碱的催化作用下可发生水解,工业上利用该反应生产肥皂 | |
| D. | 煤的气化是化学变化,石油分馏是物理变化 |
1.下列叙述正确的是( )
| A. | 碱性氧化物一定是金属氧化物 | |
| B. | 酸性氧化物一定是非金属氧化物 | |
| C. | 酸分子中有几个H原子即为几元酸 | |
| D. | 盐电离时,只生成一种阳离子,一种阴离子 |
20.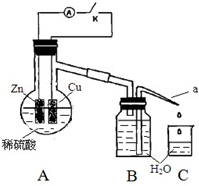 某同学分析Zn 与稀H2SO4的反应.
某同学分析Zn 与稀H2SO4的反应.
(1)该反应的离子方程式是Zn+2H+=Zn2++H2↑.
(2)制H2时,用稀硫酸而不用浓硫酸,原因是浓H2SO4具有强氧化性,不能生成氢气.
(3)已知:Zn(s)+$\frac{1}{2}$O2(g)═ZnO(s)△H=-332kJ/mol
ZnO(s)+H2SO4(aq)═ZnSO4(aq)+H2O(l)△H=-112kJ/mol
H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H=-286kJ/mol 则Zn 与稀H2SO4反应生成1mol H2时的反应热△H=kJ/mol.
(4)该同学用如下装置进行实验,分析影响反应速率的因素.
实验时,从断开K 开始,每间隔1 分钟,交替断开或闭合K,并连续计数每1 分钟内从a 管流出的水滴数,得到的水滴数如下表所示:
分析反应过程中的水滴数,请回答:
①由水滴数58>34、81>59,说明在反应初期,闭合K 时比断开K 时的反应速率快(填“快”或“慢”),主要原因是形成原电池反应速度快.
②由水滴数102>78,说明在反应后期,断开K 时的反应速率快于闭合K 时的反应速率,主要原因是断开K时,溶液中的c(H+)大于闭合K时溶液中的c(H+).
③从能量转换形式不同的角度,分析水滴数86>81、117>112 的主要原因是断开K时,反应的化学能主要转化成热能;闭合K时,反应的化学能主要转化成电能,前者使溶液的温度升得更高,故反应速率更快.
 某同学分析Zn 与稀H2SO4的反应.
某同学分析Zn 与稀H2SO4的反应.(1)该反应的离子方程式是Zn+2H+=Zn2++H2↑.
(2)制H2时,用稀硫酸而不用浓硫酸,原因是浓H2SO4具有强氧化性,不能生成氢气.
(3)已知:Zn(s)+$\frac{1}{2}$O2(g)═ZnO(s)△H=-332kJ/mol
ZnO(s)+H2SO4(aq)═ZnSO4(aq)+H2O(l)△H=-112kJ/mol
H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H=-286kJ/mol 则Zn 与稀H2SO4反应生成1mol H2时的反应热△H=kJ/mol.
(4)该同学用如下装置进行实验,分析影响反应速率的因素.
实验时,从断开K 开始,每间隔1 分钟,交替断开或闭合K,并连续计数每1 分钟内从a 管流出的水滴数,得到的水滴数如下表所示:
| 1 分钟水滴数(断开K) | 34 | 59 | 86 | 117 | … | 102 |
| 1 分钟水滴数(闭合K) | 58 | 81 | 112 | 139 | … | 78 |
①由水滴数58>34、81>59,说明在反应初期,闭合K 时比断开K 时的反应速率快(填“快”或“慢”),主要原因是形成原电池反应速度快.
②由水滴数102>78,说明在反应后期,断开K 时的反应速率快于闭合K 时的反应速率,主要原因是断开K时,溶液中的c(H+)大于闭合K时溶液中的c(H+).
③从能量转换形式不同的角度,分析水滴数86>81、117>112 的主要原因是断开K时,反应的化学能主要转化成热能;闭合K时,反应的化学能主要转化成电能,前者使溶液的温度升得更高,故反应速率更快.
17.某同学拟用重结晶的方法除去某产品中的杂质,为此要选择合适的溶剂.具有下列特点的溶剂中,不可取的溶剂是( )
| A. | 产品在溶剂中的溶解度随温度升高而迅速增大 | |
| B. | 在溶剂中产品比杂质更难溶解 | |
| C. | 杂质在溶剂中的溶解度在高温或低温时都很大 | |
| D. | 室温时产品在溶剂中很易溶解 |
16.有机物分子中原子间(或原子与原子团间)的相互影响会导致物质化学性质的不同.下列事实能说明上述观点的是( )
| A. | 乙酸易溶于水,而乙烷难溶于水 | |
| B. | 乙烯能发生加成反应,乙烷不能发生加成反应 | |
| C. | 甲苯能使高锰酸钾溶液褪色,甲烷和苯不能使高锰酸钾溶液褪色 | |
| D. | 乙醛与Ag(NH3)2 OH 1:2 反应.而甲醛为 1:4 |
15.某有机物的分子式为C3H7O2N,关于它的叙述不正确的是( )
0 158128 158136 158142 158146 158152 158154 158158 158164 158166 158172 158178 158182 158184 158188 158194 158196 158202 158206 158208 158212 158214 158218 158220 158222 158223 158224 158226 158227 158228 158230 158232 158236 158238 158242 158244 158248 158254 158256 158262 158266 158268 158272 158278 158284 158286 158292 158296 158298 158304 158308 158314 158322 203614
| A. | 该分子可能是天然蛋白质水解的产物 | |
| B. | 该分子核磁共振氢谱图可能有两个吸收峰,且面积之比为1:6 | |
| C. | 该分子只有2种同分异构体 | |
| D. | 分子中可能含有个一个羟基 |
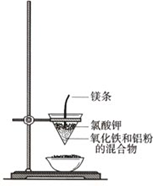 铁和铝是两种重要的金属.请回答:
铁和铝是两种重要的金属.请回答: