2.向明矾溶液中滴入氢氧化钡溶液,当SO42-沉淀完全时,铝元素的存在形式是( )
| A. | Al(OH)3 和Al3+ | B. | Al(OH)3 和AlO2- | C. | 全部为Al(OH)3 | D. | 全部为AlO2- |
1.硫酸镁和硫酸铝的混合溶液中,Al3+ 离子的浓度为0.2mol•L-1,SO42- 离子的浓度为0.4mol•L-1,则混合溶液中Mg2+离子物质的量的浓度为( )
| A. | 0.4mol•L-1 | B. | 0.3mol•L-1 | C. | 0.2mol•L-1 | D. | 0.1mol•L-1 |
20.下列物质①NaHCO3 ②(NH4)2SO4 ③Al2O3 ④(NH4)2CO3 ⑤Mg(OH)2 ⑥Fe(NO3)3中,既可以和盐酸反应也可以和Ba(OH)2溶液反应的是( )
| A. | ①③④ | B. | ①②③④ | C. | ②③④⑥ | D. | ①③④⑤ |
19.除去FeCl2溶液中混有的少量FeCl3,应选用的最佳试剂是( )
| A. | 氯水 | B. | 氢氧化钠溶液 | C. | 铜粉 | D. | 铁粉 |
18.常温下某溶液中只含有Na+、H+、OH-、A-四种离子,下列说法正确的是( )
| A. | 若溶质为NaA,溶液中可能存在:c (OH-)=c(H+)+c(HA) | |
| B. | 若c(OH-)>c(H+),溶液中不可能存在c(Na+)>c(OH-)>c(A-)>c(H+) | |
| C. | 溶液中可能存在c(Na+)>c(A-)>c(H+)>c(OH-) | |
| D. | 若溶质为NaA和HA,则一定存在c(A-)>c(Na+)>c(H+)>c(OH-) |
17.下列叙述正确的是( )
| A. | 浓度均为0.1 mol•L-1的CH3COOH和CH3COONa溶液等体积混合所得的溶液中:c(CH3COOH)+c(CH3COO-)═0.2 mol•L-1 | |
| B. | 0.1 mol•L-1 NaHCO3溶液中:c(Na+)=c(HCO3-)+c(H2CO3)+2c(CO32-) | |
| C. | 0.2 mol•L-1 HCl溶液与等体积0.1 mol•L-1 NaOH溶液混合后,溶液的pH=1 | |
| D. | 0.1 mol•L-1氨水中滴入0.1 mol•L-1盐酸至溶液呈中性时:c(NH4+)=c(Cl-) |
16.银锌碱性电池的电解质溶液为KOH溶液,电池放电时发生的总反应为Ag2O2+2Zn+4KOH+2H2O═2K2Zn(OH)4+2Ag,下列说法不正确的是( )
| A. | 放电时OH-向负极移动 | |
| B. | Ag2O2在反应中既是氧化剂又是还原剂 | |
| C. | 每生成1mol Ag外电路转移2 mol电子 | |
| D. | 负极反应为:Zn+4OH--2e-═Zn(OH)42- |
15.用以下装置和试剂构成一个原电池(如图),下列叙述正确的是( )
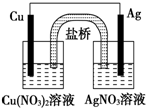

| A. | 将铜片浸入AgNO3溶液中发生的化学反应与该原电池反应相同 | |
| B. | 该电池的负极反应为:Ag++e-═Ag | |
| C. | 在外电路中,电子由银电极流向铜电极 | |
| D. | 实验过程中取出盐桥,原电池仍继续工作 |
14. 将镁条、铝条平行插入盛有一定浓度的NaOH溶液的烧杯中,用导线和电流表连接成原电池,装置如图所示.此电池工作时,下列叙述正确的是( )
将镁条、铝条平行插入盛有一定浓度的NaOH溶液的烧杯中,用导线和电流表连接成原电池,装置如图所示.此电池工作时,下列叙述正确的是( )
0 158122 158130 158136 158140 158146 158148 158152 158158 158160 158166 158172 158176 158178 158182 158188 158190 158196 158200 158202 158206 158208 158212 158214 158216 158217 158218 158220 158221 158222 158224 158226 158230 158232 158236 158238 158242 158248 158250 158256 158260 158262 158266 158272 158278 158280 158286 158290 158292 158298 158302 158308 158316 203614
 将镁条、铝条平行插入盛有一定浓度的NaOH溶液的烧杯中,用导线和电流表连接成原电池,装置如图所示.此电池工作时,下列叙述正确的是( )
将镁条、铝条平行插入盛有一定浓度的NaOH溶液的烧杯中,用导线和电流表连接成原电池,装置如图所示.此电池工作时,下列叙述正确的是( )| A. | Mg比Al活泼,Mg失去电子被氧化成Mg2+ | |
| B. | 每生成1molH2,有2mol H2O被还原 | |
| C. | 该电池的内外电路中,电流均是由电子定向移动形成的 | |
| D. | Al是电池负极,开始工作时溶液中会立即有白色沉淀析出 |