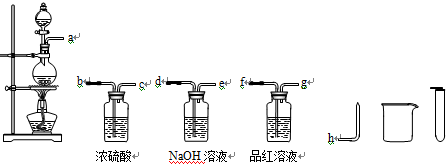
3.下列各项中前后两个叙述都正确的是( )
| A. | 单质分子中一定存在共价键;最外层有2个电子的原子都是金属原子 | |
| B. | 非极性键可以存在于离子化合物中; 质子数相同的粒子不一定属于同种元素 | |
| C. | 同位素的化学性质几乎完全相同;任何原子的原子核都是由质子和中子构成的 | |
| D. | PCl3和BCl3分子中所有原子的最外层都达到8电子稳定结构; 伴有能量变化的物质变化都是化学变化 |
2.下列排列顺序正确的是( )
①热稳定性:H2O>HF>H2S ②离子半径:F->Na+>Mg2+>Al3+
③酸性:H3PO4>H2SO4>HClO4④结合质子能力:OH->CH3COO->Cl-( )
①热稳定性:H2O>HF>H2S ②离子半径:F->Na+>Mg2+>Al3+
③酸性:H3PO4>H2SO4>HClO4④结合质子能力:OH->CH3COO->Cl-( )
| A. | ①③ | B. | ①④ | C. | ②④ | D. | ②③ |
1.下列化学用语的书写,正确的是( )
| A. | 氮气的电子式: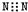 | B. | 硫原子的结构示意图: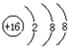 | ||
| C. | 溴化钠的电子式: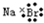 | D. | 质量数为37的氯原子${\;}_{17}^{37}$Cl |
20.某溶液在25℃时由水电离产生的H+浓度为1.0×10-12 mol/L,下列说法不正确的是( )
| A. | 该溶液的pH可能为2 | |
| B. | 若该溶液中的溶质只有一种,它可能是酸、碱或盐 | |
| C. | 向该溶液中加入铝片一定有氢气产生 | |
| D. | HSO3-、HS-、HPO42-等离子在该溶液中不能大量共存 |
19.化学在生产和日常生活中有着重要的应用.下列说法不正确的是( )
| A. | 在海轮外壳上镶入锌块,可减缓船体的腐蚀速率 | |
| B. | 电解熔融MgCl2,可制得金属镁 | |
| C. | 在铁制品上镀银时,镀件为阳极,银盐为电镀液 | |
| D. | 明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化 |
18.将一定量的锌与100mL 18.5mol/L浓硫酸充分反应,锌完全溶解,同时生成气体A 33.6L(标准状况).将反应后溶液稀释至1L,测得溶液的pH=1,下列叙述错误的是( )
| A. | 气体A为SO2和H2的混合物 | B. | 气体A中SO2与H2的体积比为5:1 | ||
| C. | 反应中共消耗Zn 97.5g | D. | 反应中共转移电子3mol |
17. 没食子儿茶素的结构如图所示,关于该物质下列叙述中正确的是( )
没食子儿茶素的结构如图所示,关于该物质下列叙述中正确的是( )
 没食子儿茶素的结构如图所示,关于该物质下列叙述中正确的是( )
没食子儿茶素的结构如图所示,关于该物质下列叙述中正确的是( )| A. | 分子式为C15H12O5 | |
| B. | 遇FeCl3溶液不发生显色反应 | |
| C. | 1mol该物质与4molNaOH恰好完全反应 | |
| D. | 易发生氧化反应和取代反应,难发生加成反应 |
16.下列说法中正确的是( )
| A. | 电子云示意图中的小黑点表示原子核最外层的电子 | |
| B. | 某元素有多种同位素,天然存在的该元素其中一种同位素的丰度为75%,则100 g天然存在的该元素中,此同位素的质量为75 g | |
| C. | 核外电子的运动状态是由该电子的电子层、电子亚层、电子云的伸展方向和电子自旋方向共同决定的 | |
| D. | 电子离核越远能量越高,所以N层电子的能量一定高于M层电子的能量 |
14.分别用等体积、等浓度的AgNO3溶液跟相同体积的下列溶液恰好完全沉淀,则下列溶液中物质的量浓度最小的是( )
0 158118 158126 158132 158136 158142 158144 158148 158154 158156 158162 158168 158172 158174 158178 158184 158186 158192 158196 158198 158202 158204 158208 158210 158212 158213 158214 158216 158217 158218 158220 158222 158226 158228 158232 158234 158238 158244 158246 158252 158256 158258 158262 158268 158274 158276 158282 158286 158288 158294 158298 158304 158312 203614
| A. | BaCl2 | B. | MgCl2 | C. | KCl | D. | FeCl3 |