19.用铝热法还原下列化合物,制得金属各1mol时,消耗铝的量最多的是( )
| A. | V2O5 | B. | Fe3O4 | C. | Cr2O3 | D. | WO3 |
18.已知正四面体形分子E和直线型分子G反应,生成四面体形分子L和直线型分子M (组成E分子的元素的原子序数小于10,组成G分子的元素为第三周期的元素).如图,则下列判断中正确的是( )
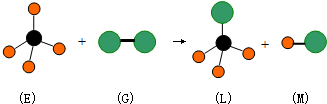

| A. | L能溶于水 | B. | M属于离子化合物 | ||
| C. | G有漂白性 | D. | 该反应是取代反应 |
17.用氧化铝为原料制取氢氧化铝最好的方法是( )
| A. | 将氧化铝粉末溶于水 | |
| B. | 将氧化铝粉末溶于盐酸,再滴入氢氧化钠溶液 | |
| C. | 将氧化铝粉末溶于氢氧化钠溶液,再滴加氨水 | |
| D. | 将氧化铝粉末溶于盐酸,再滴入过量的氨水 |
16.铝与铍的性质相似.下列关于铍的性质推断中,正确的是( )
| A. | 氯化铍的水溶液呈酸性 | B. | 氢氧化铍可溶于水 | ||
| C. | 铍只与酸反应不与碱反应 | D. | 氧化铍的化学式为Be2O3 |
15.下列只用试管和滴管就能鉴别开的一组溶液是( )
| A. | BaCl2和H2SO4 | B. | AlCl3和NH3•H2O | C. | NaCl和AgNO3 | D. | Al2(SO4)3和NaOH |
14.除去氯化铁中混有的氯化铝,最适宜的试剂组是( )
| A. | NaOH溶液、盐酸 | B. | NaOH溶液、硫酸 | C. | 氨水、NaOH溶液 | D. | 氨水、盐酸 |
13.家用液化石油气的主要成份是( )
| A. | 甲烷和乙烷 | B. | 丙烷和丁烷 | C. | 乙烷和乙烯 | D. | 戊烷和己烷 |
12.下列化学式或分子式只代表一种物质的是 ( )
| A. | C | B. | CH2Cl2 | C. | C4H10 | D. | C3H7Br |
11.下列物质属于纯净物的是( )
| A. | 硬铝 | B. | 不锈钢 | C. | 胆矾 | D. | 铝热剂 |
10.明矾[KAl(SO4)2•12H2O]在生产、生活中有广泛用途:饮用水的净化、食品工业的发酵剂等.利用炼铝厂的废料--铝灰(含Al、Al2O3及少量SiO2和FeO•xFe2O3)可制备明矾.工艺流程如下:
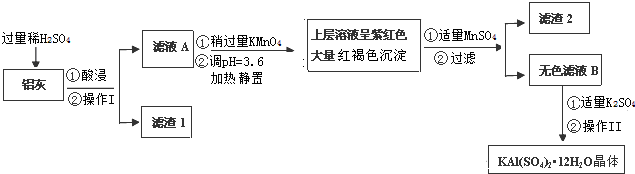
回答下列问题:
(1)明矾净水的原理是(用离子方程表示):Al3++3H2O?Al(OH)3+3H+;
(2)操作Ⅱ是:蒸发浓缩,冷却结晶、过滤、洗涤、干燥.
(3)检验滤液A中是否存在Fe2+的试剂是②(只用一种试剂,填序号)
①KSCN溶液; ②KMnO4酸性溶液; ③KI淀粉溶液.
(4)在滤液A中加入高锰酸钾发生反应的离子方程式为(该条件下Fe2+ 转化为Fe3+,MnO4-转化为Mn2+)5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O.
已知:生成氢氧化物沉淀的pH如下表所示
注:金属离子的起始浓度为0.1mol•L-1根据表中数据解释调pH=3.6的目的使Fe3+转化成Fe(OH)3沉淀,并防止Al3+沉淀.
(5)己知:在pH=3、加热条件下,MnO4-可与Mn2+反应生成MnO2.
加入MnSO4发生反应的离子方程式为:3Mn2++2MnO4-+2H2O=5MnO2+4H+.滤渣2含有的物质是MnO2、Fe(OH)3.
0 158102 158110 158116 158120 158126 158128 158132 158138 158140 158146 158152 158156 158158 158162 158168 158170 158176 158180 158182 158186 158188 158192 158194 158196 158197 158198 158200 158201 158202 158204 158206 158210 158212 158216 158218 158222 158228 158230 158236 158240 158242 158246 158252 158258 158260 158266 158270 158272 158278 158282 158288 158296 203614

回答下列问题:
(1)明矾净水的原理是(用离子方程表示):Al3++3H2O?Al(OH)3+3H+;
(2)操作Ⅱ是:蒸发浓缩,冷却结晶、过滤、洗涤、干燥.
(3)检验滤液A中是否存在Fe2+的试剂是②(只用一种试剂,填序号)
①KSCN溶液; ②KMnO4酸性溶液; ③KI淀粉溶液.
(4)在滤液A中加入高锰酸钾发生反应的离子方程式为(该条件下Fe2+ 转化为Fe3+,MnO4-转化为Mn2+)5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O.
已知:生成氢氧化物沉淀的pH如下表所示
| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀时 | 3.8 | 7.5 | 2.7 |
| 完全沉淀时 | 5.2 | 9.7 | 3.2 |
(5)己知:在pH=3、加热条件下,MnO4-可与Mn2+反应生成MnO2.
加入MnSO4发生反应的离子方程式为:3Mn2++2MnO4-+2H2O=5MnO2+4H+.滤渣2含有的物质是MnO2、Fe(OH)3.