10.已知结构为正四面体型的离子A 和直线型离子B 反应,生成三角锥形分子C 和V 形分子D(组成A、B、C、D 微粒的元素原子序数均小于10),下列说法正确的是( )


| A. | 分子C 中存在π键 | |
| B. | 微粒A 的空间结构与CH4相似,它们均为正四面体,所以它是非极性分子 | |
| C. | 固态D 的于熔沸点明显高于固态H2S 的原因在于D 分子中的共价键强于S-H 键 | |
| D. | D 分子呈V 形与其分子中存在孤对电子有关 |
8.下列说法正确的是( )
| A. | 所有的酸和碱都能使指示剂变色 | |
| B. | 物质发生缓慢氧化时一定放出热量 | |
| C. | 检测某溶液的pH时,pH试纸要预先用水湿润 | |
| D. | 一氧化碳还原氧化铜后试管壁上留下的红色物质,用稀硫酸浸泡除去 |
7.下列说法正确的是( )
| A. | H2O是一种非常稳定的化合物,这是由于氢键所致 | |
| B. | 具有相同电子层结构的四种离子A+、B2+、C-、D2-,它们的半径由大到小的顺序是D2->C->A+>B2+ | |
| C. | 分子内部一定含有共价键 | |
| D. | 族序数等于周期序数的元素一定是金属元素 |
6.如表是部分短周期元素的原子半径和主要化合价.
用化学用语回答:
(1)Z元素在周期表中的位置第三周期VIIA族.
(2)表格中是否含有短周期主族元素原子半径最大的元素是(填“是”或“否”).
(3)X和Y可以形成18e-化合物,其电子式 .
.
(4)Q元素的原子结构示意图 .
.
( 5 ) Y、M分别形成的常见氢化物沸点H2O>H2S;原因是水分子中含有氢键,故沸点高于硫化氢.
| 元素代号 | X | Y | Z | W | M | Q |
| 原子半径/nm | 0.037 | 0.074 | 0.099 | 0.186 | 0.102 | 0.143 |
| 主要化合价 | +1 | -2 | -1、+7 | +1 | -2、+6 | +3 |
(1)Z元素在周期表中的位置第三周期VIIA族.
(2)表格中是否含有短周期主族元素原子半径最大的元素是(填“是”或“否”).
(3)X和Y可以形成18e-化合物,其电子式
 .
.(4)Q元素的原子结构示意图
 .
.( 5 ) Y、M分别形成的常见氢化物沸点H2O>H2S;原因是水分子中含有氢键,故沸点高于硫化氢.
5.短周期元素X的气态氢化物的化学式为H2X,X在周期表中所在的族是( )
| A. | Ⅳ族 | B. | ⅣA 族 | C. | Ⅵ族 | D. | ⅥA族 |
4.下列有关1mol CO2的说法,正确的是( )
| A. | 质量为12 g | |
| B. | 体积为22.4 L | |
| C. | 二氧化碳分子个数约为6.02×1023个 | |
| D. | 氧原子个数约为6.02×1023个 |
2.已知某有机物A的核磁共振氢谱如图所示,下列说法中,错误的是( )
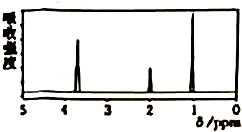

| A. | 仅由其核磁共振氢谱可知其分子中的氢原子总数由红外光谱可知,该有机物中至少含有三种不同的化学键 | |
| B. | 由核磁共振氢谱可知,该有机物分子中有三种不同的氢原子且个数比为1:2:3 | |
| C. | 若A的化学式为C3H6O2,则其结构简式为CH3COOCH3 | |
| D. | 若A的化学式为C3H6O2,则其可能的结构有三种 |
1.某化合物6.4克在氧气中完全燃烧,只生成8.8克CO2和7.2gH2O.下列说法正确的是( )
0 158087 158095 158101 158105 158111 158113 158117 158123 158125 158131 158137 158141 158143 158147 158153 158155 158161 158165 158167 158171 158173 158177 158179 158181 158182 158183 158185 158186 158187 158189 158191 158195 158197 158201 158203 158207 158213 158215 158221 158225 158227 158231 158237 158243 158245 158251 158255 158257 158263 158267 158273 158281 203614
| A. | 该化合物仅含碳、氢两种元素 | B. | 该化合物中碳氢原子个数比为1:2 | ||
| C. | 该化合约中一定含有氧元素 | D. | 若要确定其分子式一定需要质谱仪 |

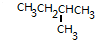 ,则该烃所有可能的结构简式为
,则该烃所有可能的结构简式为 或
或 ;
; .
. 或
或 .
. ,如果要合成
,如果要合成 所用的原始原料可以是AC
所用的原始原料可以是AC