10.为消除NO对环境的污染,可利用NH3在一定条件下与NO反应生成无污染的气体.
已知:①N2 (g)+O2 (g)?2NO(g)△H=+180.50kJ•mol-1
②4NH3 (g)+5O2 (g)?4NO(g)+6H2O(g)△H=-905.48kJ•mol-1
则反应4NH3(g)+6NO(g)?5N2 (g)+6H2O(g)的△H是( )
已知:①N2 (g)+O2 (g)?2NO(g)△H=+180.50kJ•mol-1
②4NH3 (g)+5O2 (g)?4NO(g)+6H2O(g)△H=-905.48kJ•mol-1
则反应4NH3(g)+6NO(g)?5N2 (g)+6H2O(g)的△H是( )
| A. | +2.98 kJ•mol-1 | B. | -2.98 kJ•mol-1 | ||
| C. | +1807.98 kJ•mol-1 | D. | -1807.98 kJ•mol-1 |
9.25℃时,水的电离达到平衡:H2O?H++OH-,下列叙述正确的是( )
| A. | 将水加热,Kw增大,pH不变 | |
| B. | 向水中加入少量盐酸,c(H+)增大,Kw不变 | |
| C. | 向水中加入NaOH固体,平衡逆向移动,c(OH-)降低 | |
| D. | 向水中加入AlCl3固体,平衡正向移动,c(OH-)增大 |
8.如图装置放置一段时间后,铁钉均被腐蚀.下列有关描述错误的是( )
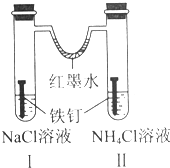

| A. | 红墨水水柱两边的液面变为左低右高 | |
| B. | Ⅰ和Ⅱ中负极反应式均为Fe-2e-=Fe2+ | |
| C. | Ⅰ中正极反应式为O2+2H2O+4e-=4OH- | |
| D. | Ⅱ中加入少量K3[Fe(CN)6]溶液,生成蓝色沉淀 |
7.一定条件下,容积为1L的密闭容器中发生反应:
SiF4(g)+2H2O(g)?SiO2(s)+4HF(g)△H=+148.9kJ•mol-1
下列各项中不能说明该反应已达化学平衡状态的是( )
SiF4(g)+2H2O(g)?SiO2(s)+4HF(g)△H=+148.9kJ•mol-1
下列各项中不能说明该反应已达化学平衡状态的是( )
| A. | v(SiF4)消耗=4v(HF)生成 | B. | HF的体积分数不再变化 | ||
| C. | 容器内气体压强不再变化 | D. | 容器内气体的总质量不再变化 |
6.25℃时,浓度相同的Na2CO3和NaHCO3溶液,下列判断不正确的是( )
| A. | 粒子种类不相同 | B. | c(OH-)前者大于后者 | ||
| C. | 均存在电离平衡和水解平衡 | D. | 分别加入NaOH固体,c(CO32-)均增大 |
5.下列解释事实的离子方程式不正确的是( )
| A. | 粗铜精炼时,阴极质量增加:Cu2++2e-═Cu | |
| B. | 明矾可用作净水剂:Al3++3H2O═Al(OH)3↓+3H+ | |
| C. | 用食醋除去水壶中的水垢(CaCO3):2CH3COOH+CaCO3═Ca2++2CH3COO-+CO2↑+H2O | |
| D. | 向氢氧化镁浊液中滴入酚酞溶液,溶液变红:Mg(OH)2(s)?Mg2+(aq)+2OH- (aq) |
4.配制FeCl3溶液时,为防止出现浑浊,可向该溶液中加入少量( )
| A. | 铁 | B. | 盐酸 | C. | 氯化钠 | D. | 氢氧化钠 |
3.在电解水制取H2和O2时,为了增强液体的导电性,可加入下列物质中的( )
| A. | HCl | B. | CuCl2 | C. | NaOH | D. | CuSO4 |
1. 如图是以Zn和Cu为电极,稀H2SO4为电解质溶液形成的原电池,某实验兴趣小组做完实验后,在读书卡片上记录如下:
如图是以Zn和Cu为电极,稀H2SO4为电解质溶液形成的原电池,某实验兴趣小组做完实验后,在读书卡片上记录如下:
(1)卡片中记录合理的是③④⑥(填序号).
(2)该电池总反应的离子方程式是Zn+2H+=Zn2++H2↑.
(3)在实验中铜片上有气泡产生原因是锌较活泼,在负极发生氧化反应失去电子,电子由导线流向铜电极,氢离子在铜表面得到电子生成氢气.
(4)若将稀硫酸换成硫酸铜溶液,电极质量增加的是铜极(填“锌极”或“铜极”),原因是Cu2++2e-=Cu(用电极方程式表示).
0 158075 158083 158089 158093 158099 158101 158105 158111 158113 158119 158125 158129 158131 158135 158141 158143 158149 158153 158155 158159 158161 158165 158167 158169 158170 158171 158173 158174 158175 158177 158179 158183 158185 158189 158191 158195 158201 158203 158209 158213 158215 158219 158225 158231 158233 158239 158243 158245 158251 158255 158261 158269 203614
 如图是以Zn和Cu为电极,稀H2SO4为电解质溶液形成的原电池,某实验兴趣小组做完实验后,在读书卡片上记录如下:
如图是以Zn和Cu为电极,稀H2SO4为电解质溶液形成的原电池,某实验兴趣小组做完实验后,在读书卡片上记录如下:| ①Zn为正极,Cu为负极; ②H+向负极移动; ③Cu极有H2产生; ④电子流动方向Zn→G→Cu; ⑤正极的电极反应式是Zn-2e-=Zn2+: ⑥若有1mol电子流过导线,则理论上产生0.5mol H2. |
(2)该电池总反应的离子方程式是Zn+2H+=Zn2++H2↑.
(3)在实验中铜片上有气泡产生原因是锌较活泼,在负极发生氧化反应失去电子,电子由导线流向铜电极,氢离子在铜表面得到电子生成氢气.
(4)若将稀硫酸换成硫酸铜溶液,电极质量增加的是铜极(填“锌极”或“铜极”),原因是Cu2++2e-=Cu(用电极方程式表示).