1.下表是元素周期表的一部分.
(1)表中元素⑩的氢化物的化学式为HCl,此氢化物的还原性比元素⑨的氢化物的还原性弱(填强或弱).
(2)在⑦、⑧、⑨、⑩4种元素中,原子半径最大的是Mg(填元素符号),其原子结构示意图为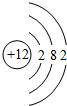 .
.
(3)写出⑤元素的最高价氧化物的水化物与其气态氢化物发生反应的化学方程式:NH3+HNO3═NH4NO3.
(4)写出元素⑦的氯化物的水溶液与NaOH溶液反应的离子方程式:Mg2++2OH-═Mg(OH)2↓.
(5)要证明⑥元素比⑨元素的氧化性强的化学方程式为:2H2S+O2═2H2O+2S↓.
主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA |
| 1 | ① | ||||||
| 2 | ② | ③ | ④ | ⑤ | ⑥ | ||
| 3 | ⑦ | ⑧ | ⑨ | ⑩ |
(2)在⑦、⑧、⑨、⑩4种元素中,原子半径最大的是Mg(填元素符号),其原子结构示意图为
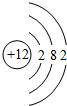 .
.(3)写出⑤元素的最高价氧化物的水化物与其气态氢化物发生反应的化学方程式:NH3+HNO3═NH4NO3.
(4)写出元素⑦的氯化物的水溶液与NaOH溶液反应的离子方程式:Mg2++2OH-═Mg(OH)2↓.
(5)要证明⑥元素比⑨元素的氧化性强的化学方程式为:2H2S+O2═2H2O+2S↓.
20.如图是元素周期表的一部分.X、Y、Z、W均为短周期元素,Z元素原子最外层电子数是电子层数的2倍.下列说法不正确的是( )
| X | Y | ||
| Z | W |
| A. | W 的最高价氧化物的水化物酸性比Z的强 | |
| B. | 原子半径:Z>W,离子半径:Z<W | |
| C. | Y的气态氢化物可与W的气态氢化物反应生成一种离子化合物 | |
| D. | X元素形成的化合物种类最多 |
19.反应 4NH3(气)+5O2(气)?4NO(气)+6H2O(气),在2L的密闭容器中进行,2min后,NH3减少了0.12mol,则平均每min浓度变化正确的是( )
| A. | NH3:0.12 mol•L-1 | B. | H2O:0.09 mol•L-1 | ||
| C. | NO:0.03 mol•L-1 | D. | O2:0.15 mol•L-1 |
18.杜布纳联合研究所使用粒子回旋加速器,用${\;}_{20}^{48}$Ca轰击${\;}_{97}^{249}$Bk(锫)生成${\;}_{117}^{293}$UP和${\;}_{117}^{294}$UP,Up就是科学家一直寻找的第117号元素.下列有关说法正确的是( )
| A. | ${\;}_{97}^{249}$Bk(锫)中的中子数为97 | |
| B. | ${\;}_{117}^{293}$UP和${\;}_{117}^{294}$UP互为同位素 | |
| C. | 用 ${\;}_{20}^{48}$Ca轰击${\;}_{97}^{249}$Bk的变化是化学变化 | |
| D. | ${\;}_{20}^{48}$Ca、${\;}_{97}^{249}$Bk、${\;}_{117}^{293}$UP、${\;}_{117}^{294}$UP属于四种元素 |
17. 碳酸钠在不同温度下可以失去部分或全部的结晶水,现有一种碳酸钠晶体(Na2CO3•nH2O)样品,可采用在不同温度下加热样品(温度逐渐升高)来测定其组成.
碳酸钠在不同温度下可以失去部分或全部的结晶水,现有一种碳酸钠晶体(Na2CO3•nH2O)样品,可采用在不同温度下加热样品(温度逐渐升高)来测定其组成.
(1)某学生的实验流程如下:

①称量用的仪器是托盘天平,最小量度单位0.1g.
②如图为灼烧装置.下列对应仪器的名称中,若正确的在后面横线上写上“正确”,若错误请将正确名称写在后面横线上.
a.坩锅正确 b.三脚架泥三角
③流程中“操作”是指冷却,这一操作必须放在干燥器(填仪器名称)中进行.
④该学生停止实验的依据为连续两次称量的质量差不超过0.1g.
⑤实验结果记录如下:容器质量为33.6g
根据上表数据推算出n值,n=10.
(2)另有学生测定结果n值偏小,其可能的原因为b、c.
a.温度过高致少量碳酸钠分解了 b.碳酸钠晶体样品已有少量风化
c.碳酸钠晶体样品没有完全失去结晶水 d.加热过程中有少量晶体溅出.
 碳酸钠在不同温度下可以失去部分或全部的结晶水,现有一种碳酸钠晶体(Na2CO3•nH2O)样品,可采用在不同温度下加热样品(温度逐渐升高)来测定其组成.
碳酸钠在不同温度下可以失去部分或全部的结晶水,现有一种碳酸钠晶体(Na2CO3•nH2O)样品,可采用在不同温度下加热样品(温度逐渐升高)来测定其组成.(1)某学生的实验流程如下:

①称量用的仪器是托盘天平,最小量度单位0.1g.
②如图为灼烧装置.下列对应仪器的名称中,若正确的在后面横线上写上“正确”,若错误请将正确名称写在后面横线上.
a.坩锅正确 b.三脚架泥三角
③流程中“操作”是指冷却,这一操作必须放在干燥器(填仪器名称)中进行.
④该学生停止实验的依据为连续两次称量的质量差不超过0.1g.
⑤实验结果记录如下:容器质量为33.6g
| 称量次序 | 加热温度(℃) | 容器+试样质量(g) |
| Ⅰ | 常温 | 62.2 |
| Ⅱ | T1 | 56.8 |
| Ⅲ | T2 | 49.6 |
| Ⅳ | T3 | 44.2 |
| Ⅴ | T4 | 44.2 |
(2)另有学生测定结果n值偏小,其可能的原因为b、c.
a.温度过高致少量碳酸钠分解了 b.碳酸钠晶体样品已有少量风化
c.碳酸钠晶体样品没有完全失去结晶水 d.加热过程中有少量晶体溅出.
16.五千多年前,人类就开始了对铁的使用.下列有关铁的说法中正确的是( )
| A. | 工业上通常把金属分为黑色金属和有色金属,铁属于黑色金属,是因为铁是黑色的 | |
| B. | 常温下,铁制容器可以用来贮存浓硫酸 | |
| C. | 铁的最高价是+3价,是因为铁原子的最外层有3个电子 | |
| D. | 在地壳中铁大多以游离态存在 |
15.有甲、乙、丙三瓶等体积等物质的量浓度的NaOH溶液.若将甲蒸发掉一半水,在乙中通入少量CO2,丙不变.然后用同浓度H2SO4溶液滴定,完全反应生成Na2SO4,所需H2SO4溶液的体积是( )
| A. | 甲=丙>乙 | B. | 丙>乙>甲 | C. | 乙>丙>甲 | D. | 甲=乙=丙 |
14.测定1mol氢气的体积时,以下操作使测定结果偏大的是( )
| A. | 装置漏气 | |
| B. | 镁带称量后擦去表面氧化膜 | |
| C. | 测定时氢气的实际温度高于记录温度数值 | |
| D. | 镁带中含有不溶于酸的杂质 |
13.在实验室里可按图所示的装置来干燥、收集气体R,多余的气体R可用水吸收,则R是( )


| A. | HCl | B. | Cl2 | C. | NH3 | D. | CO |
12.X、Y是第三周期的非金属元素,X原子半径比Y原子半径大,则下列叙述中正确的是( )
0 158065 158073 158079 158083 158089 158091 158095 158101 158103 158109 158115 158119 158121 158125 158131 158133 158139 158143 158145 158149 158151 158155 158157 158159 158160 158161 158163 158164 158165 158167 158169 158173 158175 158179 158181 158185 158191 158193 158199 158203 158205 158209 158215 158221 158223 158229 158233 158235 158241 158245 158251 158259 203614
| A. | X的最高价氧化物对应水化物的酸性比Y的最高价氧化物对应水化物的酸性强 | |
| B. | X原子的得电子能力比Y原子的得电子能力强 | |
| C. | X的阴离子的还原性比Y的阴离子的还原性强 | |
| D. | X的气态氢化物比Y的气态氢化物稳定 |