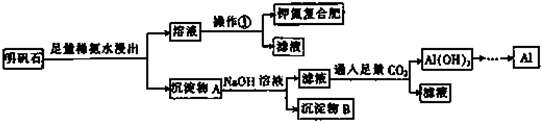
10.我国科学家研制出一中催化剂,能在室温下高效催化空气中甲醛的氧化,其反应如下:HCHO+O2$\stackrel{催化剂}{→}$CO2+H2O.下列有关说法正确的是( )
| A. | 反应物和生成物都是非极性分子 | |
| B. | 0.5molHCHO 含有1molσ键 | |
| C. | HCHO、CO2分子中中心原子杂化类型相 | |
| D. | 液态水中只存在一种作用力同 |
9.某物质的结构为: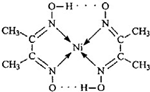 .对该物质的分析判断正确的是( )
.对该物质的分析判断正确的是( )
 .对该物质的分析判断正确的是( )
.对该物质的分析判断正确的是( )| A. | 该物质是中不存在σ键 | |
| B. | 该物质的分子中只含有共价键、配位键两种作用力 | |
| C. | 该物质是一种配合物,其中N 原子为配位体 | |
| D. | 该物质中C、N、O 原子存在孤对电子 |
8.短周期主族元素W、X、Y、Z 的原子序数依次增大,W、X 原子的最外层电子数之比为4:3,Z 原子比X 原子的核外电子数多4.下列说法正确的是( )
| A. | W、Y、Z 的电负性大小顺序一定是Z>Y>W | |
| B. | Z 的氢化物分之间存在氢键 | |
| C. | Y、Z 形成的分子的中心原子可能采用sp3杂化 | |
| D. | WY2分子中σ键与π键的数目之比是2:1 |
7.某温度下.在一容积不变的密闭容器中充入2molSO2和1molO2,一段时间后反应达到平衡状态,测得平衡时的压强为反应前的0.8倍.则SO2的转化率为( )
| A. | 20% | B. | 40% | C. | 60% | D. | 80% |
4.下列判断正确的是( )
| A. | 欲配制1.00 L 1.00 mol•L-1的NaCl溶液,可将58.5 g NaCl溶于1.00 L水中 | |
| B. | 将80 g SO3溶于水并配成1 L溶液,溶质的物质的量浓度为1 mol•L-1 | |
| C. | 10 mL质量分数为98%的H2SO4,用水稀释至100 mL,H2SO4的质量分数为9.8% | |
| D. | 1 mol•L-1 NaCl溶液含有NA个Na+ |
3.下列有关比较中,大小顺序排列不正确的是( )
0 158062 158070 158076 158080 158086 158088 158092 158098 158100 158106 158112 158116 158118 158122 158128 158130 158136 158140 158142 158146 158148 158152 158154 158156 158157 158158 158160 158161 158162 158164 158166 158170 158172 158176 158178 158182 158188 158190 158196 158200 158202 158206 158212 158218 158220 158226 158230 158232 158238 158242 158248 158256 203614
| A. | 热稳定性:HF>H2O>NH3>CH4 | |
| B. | 离子半径:S2->K+>Na+>Al3+ | |
| C. | 碱性:Mg(OH)2<KOH<CsOH | |
| D. | 给出质子的能力:H3PO4<H2SO4<HClO |
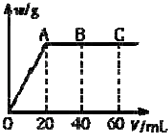 有H2SO4和HCl 的混合溶液20mL,加入0.025mol•L-1 Ba(OH)2溶液时,生成沉淀的质量w(g)和Ba(OH)2溶液的体积V(mL)的关系如图所示(C 点混合液pH=7).
有H2SO4和HCl 的混合溶液20mL,加入0.025mol•L-1 Ba(OH)2溶液时,生成沉淀的质量w(g)和Ba(OH)2溶液的体积V(mL)的关系如图所示(C 点混合液pH=7).