1.在一定温度下,反应$\frac{1}{2}$H2(g)$+\frac{1}{2}$X2(g)?HX(g)的平衡常数为9.若将1.0mol的HX(g)通入体积为1.0L的密闭容器中,在该温度时HX(g)的最大分解率接近于( )
| A. | 10% | B. | 18% | C. | 20% | D. | 40% |
20.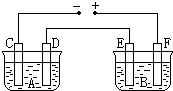 如图所示,A池用石墨电极电解氢氧化钠溶液,B池精炼粗铜.一段时间后停止通电,A池D极产生的气体在标准状况下为2.24L,则B池中E极质量的变化是( )
如图所示,A池用石墨电极电解氢氧化钠溶液,B池精炼粗铜.一段时间后停止通电,A池D极产生的气体在标准状况下为2.24L,则B池中E极质量的变化是( )
 如图所示,A池用石墨电极电解氢氧化钠溶液,B池精炼粗铜.一段时间后停止通电,A池D极产生的气体在标准状况下为2.24L,则B池中E极质量的变化是( )
如图所示,A池用石墨电极电解氢氧化钠溶液,B池精炼粗铜.一段时间后停止通电,A池D极产生的气体在标准状况下为2.24L,则B池中E极质量的变化是( )| A. | 质量增加6.4 g | B. | 质量增加12.8 g | C. | 质量减少6.4 g | D. | 质量减少12.8 g |
19.已知:4P(红磷,S)═P4(白磷,s)△H=+17kJ•moL-1,则下列推论正确的是( )
| A. | 当1 mol白磷完全转变成红磷时放出17kJ热量 | |
| B. | 正反应是一个放热反应 | |
| C. | 当4g红磷转变成白磷时吸收I7k J热量 | |
| D. | 白磷比红磷稳定 |
18.食品安全日益受到人们的关注.下列食品能食用的是( )
| A. | 使用瘦肉精饲养的猪 | B. | 用着色剂染色的馒头 | ||
| C. | 用硫酸铜浸泡过粽叶的粽子 | D. | 用食盐水浸泡过的菠萝 |
17.下列食品你认为长期食用对人体有益无害的是( )
| A. | 油炸薯条 | B. | 碳酸饮料 | C. | 烤羊肉串 | D. | 新鲜蔬菜 |
16. 电导率可用于衡量电解质溶液导电能力大小.室温下,用0.100mol•L-lNH3•H2O滴定 10.00mL浓度均为 0.100mol•L-l HCl和CH3COOH的混合溶液,所得曲线如图所示.下列说法正确的是( )
电导率可用于衡量电解质溶液导电能力大小.室温下,用0.100mol•L-lNH3•H2O滴定 10.00mL浓度均为 0.100mol•L-l HCl和CH3COOH的混合溶液,所得曲线如图所示.下列说法正确的是( )
 电导率可用于衡量电解质溶液导电能力大小.室温下,用0.100mol•L-lNH3•H2O滴定 10.00mL浓度均为 0.100mol•L-l HCl和CH3COOH的混合溶液,所得曲线如图所示.下列说法正确的是( )
电导率可用于衡量电解质溶液导电能力大小.室温下,用0.100mol•L-lNH3•H2O滴定 10.00mL浓度均为 0.100mol•L-l HCl和CH3COOH的混合溶液,所得曲线如图所示.下列说法正确的是( )| A. | ①点溶液中c (H+)为0.200 mol•L-l | |
| B. | 若反应容器与外界没有热交换,反应后溶液温度高低为①>③>② | |
| C. | pH的大小为:③>②>①,且③点溶液中有c(Cl-)>c(CH3COO-) | |
| D. | ③点后因离子数目减少使溶液电导率略降低 |
15.一定条件下,反应:C(s)+CO2(g)?2CO(g)在2L恒容密闭容器中进行,反应进行20s时,CO的物质的量增加了0.40mol,则下列说法正确的是( )
| A. | 该反应是一熵减反应 | |
| B. | 升高温度时,反应向逆方向进行 | |
| C. | 反应平衡时,v (CO2):v (CO)=1:2 | |
| D. | 充入N2使体系压强增大,能提高反应速率 |
14.低脱硝技术可用于处理废气中的氮氧化物,发生的化学反应为:2NH3(g)+NO(g)+NO2(g)$\stackrel{催化剂}{?}$2N2(g)+3H2O(g)△H<0.在恒容的密闭容器中,下列有关说法正确的是( )
| A. | 平衡时,其他条件不变,增加NH3的浓度,反应速率会降低 | |
| B. | 单位时间内消耗NO和N2的物质的量比为1:2时,反应达到平衡 | |
| C. | 其他条件不变,充入氦气,压强增大,化学反应速率增大 | |
| D. | 平衡时,其他条件不变,升高温度可使该反应的平衡常数增大 |
13.向5mL NaCl溶液中滴入一滴AgNO3溶液,出现白色沉淀,继续滴加一滴KI溶液并振荡,沉淀变为黄色,再滴入一滴Na2S溶液并振荡,沉淀又变成黑色,根据上述变化过程,分析此三种沉淀物的溶度积关系为( )
0 158055 158063 158069 158073 158079 158081 158085 158091 158093 158099 158105 158109 158111 158115 158121 158123 158129 158133 158135 158139 158141 158145 158147 158149 158150 158151 158153 158154 158155 158157 158159 158163 158165 158169 158171 158175 158181 158183 158189 158193 158195 158199 158205 158211 158213 158219 158223 158225 158231 158235 158241 158249 203614
| A. | AgCl=AgI=Ag2S | B. | AgCl<AgI<Ag2S | C. | AgI>AgCl>Ag2S | D. | AgCl>AgI>Ag2S |