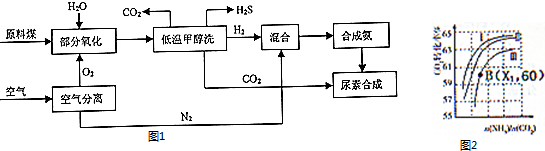
11.小组同学将铜片加入稀硝酸,发现开始时反应非常慢,一段时间后反应速率明显加快.该小组通过实验探究其原因.请你和探究小组完成下列问题:
(1)提出合理假设.该实验中反应速率明显加快的原因可能是AC.
A.反应放热导致温度升高 B.压强增大
C.生成物的催化作用 D.反应物接触面积增大
(2)初步探究测定实验过程中不同时间溶液的温度,结果如表:
根据表中实验数据规律,结合实验假设你能得出的结论是温度不是反应速率明显加快的主要原因.
(3)进一步探究.查阅文献了解到化学反应的产物(含中间产物)可能对反应有催化作用.为此,请你完成以下实验设计(将表格和实验目的补充完整):
表中X的值为,实验①和②探究Cu2+对实验的影响.
(1)提出合理假设.该实验中反应速率明显加快的原因可能是AC.
A.反应放热导致温度升高 B.压强增大
C.生成物的催化作用 D.反应物接触面积增大
(2)初步探究测定实验过程中不同时间溶液的温度,结果如表:
| 时间/min | 0 | 5 | 10 | 15 | 20 | 25 | 35 | 50 | 60 | 70 | 80 |
| 温度/℃ | 25 | 26 | 26 | 26 | 26 | 26 | 26.5 | 27 | 27 | 27 | 27 |
(3)进一步探究.查阅文献了解到化学反应的产物(含中间产物)可能对反应有催化作用.为此,请你完成以下实验设计(将表格和实验目的补充完整):
| 实验 编号 | 铜片 质量/g | 0.1mol•L-1 硝酸/mL | 硝酸铜 溶液/mL | 亚硝酸钠 溶液/mL | 水的体积 /mL | 实验目的 |
| ① | 5 | 20 | 0 | 0 | 0.5 | 实验①和②探究Cu2+对实验的影响;实验①和③探究亚硝酸根的影响. |
| ② | 5 | 20 | 0.5 | 0 | 0 | |
| ③ | 5 | 20 | 0 | X | 0 |
8.控制变量法是研究化学变化量的重要思想方法.请仔细观察表中50mL稀盐酸和1g碳酸钙反应的实验数据:
(1)该反应属于放热反应(填“吸热”或“放热”).
(2)实验5、6表明温度 对反应速率的影响.
(3)从本实验数据中分析,影响化学反应速率的因素还有反应物接触面积,能表明这一规律的实验序号是1、2.
| 实验 序号 | 碳酸钙 状态 | C(HCl)/mol•l-1 | 溶液温度/℃ | 碳酸钙消失 时间/s | |
| 反应前 | 反应后 | ||||
| 1 | 块状 | 0.5 | 20 | 39 | 400 |
| 2 | 粉末 | 0.5 | 20 | 40 | 60 |
| 3 | 块状 | 0.6 | 20 | 41 | 280 |
| 4 | 粉末 | 0.8 | 20 | 40 | 30 |
| 5 | 块状 | 1.0 | 20 | 40 | 120 |
| 6 | 块状 | 1.0 | 30 | 50 | 40 |
(2)实验5、6表明温度 对反应速率的影响.
(3)从本实验数据中分析,影响化学反应速率的因素还有反应物接触面积,能表明这一规律的实验序号是1、2.
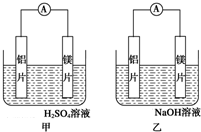
2.已知lg3=0.48,25℃时NH3•H2O的电离平衡常数为1.8×10-5,现向0.2mol/L的氨水中滴加等体积的0.1mol/L的盐酸得到新溶液Q,下列有关说法中错误的是( )
0 158054 158062 158068 158072 158078 158080 158084 158090 158092 158098 158104 158108 158110 158114 158120 158122 158128 158132 158134 158138 158140 158144 158146 158148 158149 158150 158152 158153 158154 158156 158158 158162 158164 158168 158170 158174 158180 158182 158188 158192 158194 158198 158204 158210 158212 158218 158222 158224 158230 158234 158240 158248 203614
| A. | 此氨水的pH为11.48 | |
| B. | Q溶液中:c(NH4+)>c(Cl-)>c(NH3•H2O)>c(OH-)>c(H+) | |
| C. | Q溶液中:2c(Cl-)=c(NH3•H2O)+c(NH4+) | |
| D. | 滴加过程中,溶液中可能会存在:c(NH4+)=c(Cl-) |
 有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均用镁片和铝片作电极,但甲同学将电极放入6mol•L-1的H2SO4溶液中,乙同学将电极放入6mol•L-1的NaOH溶液中,如图所示.
有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均用镁片和铝片作电极,但甲同学将电极放入6mol•L-1的H2SO4溶液中,乙同学将电极放入6mol•L-1的NaOH溶液中,如图所示.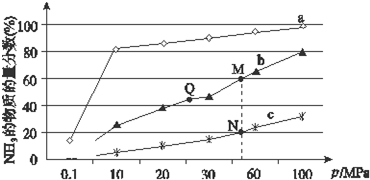
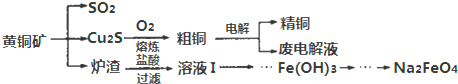
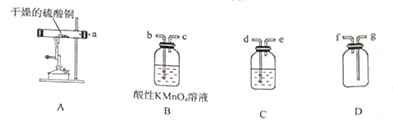 CuSO4•5H2O是铜的重要化合物,有着广泛的应用.硫酸铜在高温下分解可得到SO2、SO3、O2和Cu2O.
CuSO4•5H2O是铜的重要化合物,有着广泛的应用.硫酸铜在高温下分解可得到SO2、SO3、O2和Cu2O.