20.某学习小组在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率.为了进一步研究硫酸铜的量对氢气生成速率的影响,该小组同学开始了实验探究.
(1)实验方案:将表中所给的混合溶液分别加入到6个盛有过量Zn粒的锥形瓶中,收集产生的气体.记录单位时间氢气产生的体积.
其中:V1=30,V6=10,V9=17.5;
(2)实验装置:甲同学拟选用下列实验装置完成实验:

①你认为最简易的装置其连接顺序是:A接E接D接G(填接口字母,可不填满.)
②实验开始时,先打开分液漏斗上口的玻璃塞,再轻轻打开其活塞,一会儿后稀硫酸就不能顺利滴入锥形瓶.请你帮助分析原因.
③实验最后,在读取测量实验中生成氢气的总体积时,你认为合理的是.
A.待实验装置冷却后再读数
B.上下移动量筒F,使其中液面与广口瓶中液面相平
C.上下移动量筒G,使其中液面与广口瓶中液面相平
D.视线与凹液面的最低点水平读取量筒中水的体积
(3)问题讨论:实验室中现有Na2SO4、MgSO4、Ag2SO4、K2SO4等4种溶液,可与实验中CuSO4溶液起相似作用的是Ag2SO4;要加快上述实验中气体产生的速率,还可采取的措施有升高反应温度;适当增加硫酸的浓度(答两种).
(1)实验方案:将表中所给的混合溶液分别加入到6个盛有过量Zn粒的锥形瓶中,收集产生的气体.记录单位时间氢气产生的体积.
| 实验混合溶液 | A | B | C | D | E | F |
| 4mol/LH2SO4/mL | 30 | V1 | V2 | V3 | V4 | V5 |
| 饱和CuSO4溶液/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
(2)实验装置:甲同学拟选用下列实验装置完成实验:

①你认为最简易的装置其连接顺序是:A接E接D接G(填接口字母,可不填满.)
②实验开始时,先打开分液漏斗上口的玻璃塞,再轻轻打开其活塞,一会儿后稀硫酸就不能顺利滴入锥形瓶.请你帮助分析原因.
③实验最后,在读取测量实验中生成氢气的总体积时,你认为合理的是.
A.待实验装置冷却后再读数
B.上下移动量筒F,使其中液面与广口瓶中液面相平
C.上下移动量筒G,使其中液面与广口瓶中液面相平
D.视线与凹液面的最低点水平读取量筒中水的体积
(3)问题讨论:实验室中现有Na2SO4、MgSO4、Ag2SO4、K2SO4等4种溶液,可与实验中CuSO4溶液起相似作用的是Ag2SO4;要加快上述实验中气体产生的速率,还可采取的措施有升高反应温度;适当增加硫酸的浓度(答两种).
19.下列分子中所有原子都满足最外层为8电子结构的是( )
| A. | PCl5 | B. | BF3 | C. | CCl4 | D. | NH3 |
17.煤、石油、天然气是人类使用的主要能源,同时也是重要的化工原料.下列关于它们的综合利用叙述不正确的是( )
| A. | 以煤、石油和天然气为主要原料生产的合成材料是塑料、合成橡胶、合成纤维 | |
| B. | 煤是工业上获得芳香烃的一种重要来源 | |
| C. | 石油的裂解是为了提高轻质油(例如汽油)的产量 | |
| D. | 天然气的主要成分是甲烷,属于不可再生资源 |
16.患甲状腺肿大的病人需补充的元素是( )
| A. | 铁元素 | B. | 钙元素 | C. | 碘元素 | D. | 镁元素 |
15.实验测得-25℃时干冰晶体(面心结构)的晶胞边长为acm,其摩尔质量为Mg/mol,则该干冰晶体的密度为(单位:g/cm3)( )
| A. | $\frac{14M}{{a}^{3}{N}_{A}}$ | B. | $\frac{M}{{a}^{3}{N}_{A}}$ | C. | $\frac{2M}{{a}^{3}{N}_{A}}$ | D. | $\frac{4M}{{a}^{3}{N}_{A}}$ |
14.物质的结构决定物质的性质.请回答下列涉及物质结构和性质的问题: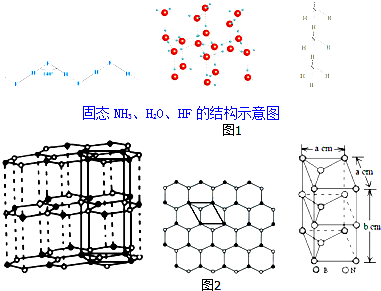
(1)基态Cu2+的电子排布式为1s22s22p63s23p63d9,其最外电子层的电子数为17.
(2)利用价层电子对互斥理论(VSEPR theory)预测多原子分子或离子立体构型时,认为价层电子间互斥力(F)的大小决定了夹角(∠)的大小:F(孤电子对间)>F(孤电子对-双键电子)>F(双键电子-单键电子)>F(单键电子间),则a.∠(孤-孤夹角)、b.∠(孤-双夹角)、c.∠(双-单夹角)、d.∠(单-单夹角)由大到小的排序为abcd(填编号);XeF4中Xe价层电子数为6对,画出其VSEPR模型(含中心原子的孤电子对)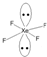 .
.
(3)在图1中,除NH3、H2O、HF外的同主族氢化物的沸点随周期数增大而升高的原因是同为分子晶体,物质的组成与结构相似,相对分子质量越大,分子间作用力越大;
已知固态NH3、H2O、HF的氢键键能和结构如表:
根据如表固态NH3、H2O、HF的结构示意图解释H2O、HF、NH3沸点依次降低的原因:单个氢键的键能是(HF)n>冰>(NH3)n,而平均每个分子含氢键数:冰中2个,(HF)n和(NH3)n只有1个,气化要克服的氢键的总键能是冰>(HF)n>(NH3)n.
(4)石墨型BN呈白色,亦称“白石墨”,“白石墨”在一定条件下可转化为金刚石型BN.“白石墨”的结构示意图和晶胞如图2(中图是晶胞底面从“白石墨”中的截取情况),则“白石墨”的密度为$\frac{100}{\sqrt{3}{N}_{A}{a}^{2}b}$g•cm-3(以含a、b的代数式表示).
0 158031 158039 158045 158049 158055 158057 158061 158067 158069 158075 158081 158085 158087 158091 158097 158099 158105 158109 158111 158115 158117 158121 158123 158125 158126 158127 158129 158130 158131 158133 158135 158139 158141 158145 158147 158151 158157 158159 158165 158169 158171 158175 158181 158187 158189 158195 158199 158201 158207 158211 158217 158225 203614

(1)基态Cu2+的电子排布式为1s22s22p63s23p63d9,其最外电子层的电子数为17.
(2)利用价层电子对互斥理论(VSEPR theory)预测多原子分子或离子立体构型时,认为价层电子间互斥力(F)的大小决定了夹角(∠)的大小:F(孤电子对间)>F(孤电子对-双键电子)>F(双键电子-单键电子)>F(单键电子间),则a.∠(孤-孤夹角)、b.∠(孤-双夹角)、c.∠(双-单夹角)、d.∠(单-单夹角)由大到小的排序为abcd(填编号);XeF4中Xe价层电子数为6对,画出其VSEPR模型(含中心原子的孤电子对)
 .
.(3)在图1中,除NH3、H2O、HF外的同主族氢化物的沸点随周期数增大而升高的原因是同为分子晶体,物质的组成与结构相似,相对分子质量越大,分子间作用力越大;
已知固态NH3、H2O、HF的氢键键能和结构如表:
| 物质 | 氢键X-H…Y | 键能/kJ•mol-1 |
| (HF)n | F-H…F | 28.1 |
| 冰 | O-H…O | 18.8 |
| (NH3)n | N-H…N | 5.4 |
(4)石墨型BN呈白色,亦称“白石墨”,“白石墨”在一定条件下可转化为金刚石型BN.“白石墨”的结构示意图和晶胞如图2(中图是晶胞底面从“白石墨”中的截取情况),则“白石墨”的密度为$\frac{100}{\sqrt{3}{N}_{A}{a}^{2}b}$g•cm-3(以含a、b的代数式表示).
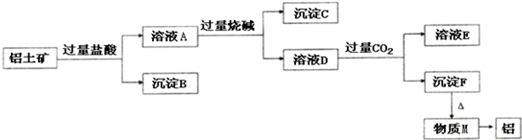

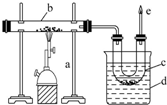 图是实验室干馏煤的装置图,回答下列问题:
图是实验室干馏煤的装置图,回答下列问题: