16.下列叙述中正确的是( )
| A. | 在元素周期表中,零族元素的单质在常温下全部都是气体 | |
| B. | 同周期元素,ⅦA族的原子半径最大 | |
| C. | ⅥA族元素的原子,其半径越大,越容易失去电子 | |
| D. | 所有主族元素的原子形成单原子离子时的最高化合价数都和它的族序数相等 |
15.随着手机、手提电脑、数码相机等电器的普及,锂电池的生产量和消费量大.造成资源短缺,钴的毒性又很大.因此,回收锂电池既有较大的经济价值,又有益于保护生态环境.某课题小组提出如下方案对某钴酸锂正极材料(主要含LiCoO2、铝箔、性质稳定的导电剂等)进行回收钴等金属.
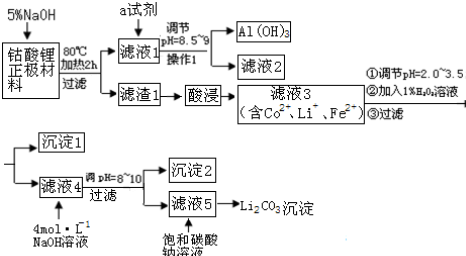
已知:金属氢氧化物沉淀的pH值
回答下列问题:
(1)写出钴酸锂正极材料用加5%氢氧化钠溶液,发生的离子反应方程式2Al+2OH-+2H2O=2AlO2-+3H2↑
(2)操作1所用到的玻璃仪器除烧杯、漏斗外,还必须有玻璃棒(填仪器名称).
(3)滤液4到沉淀2可以选择抽滤,抽滤不仅能加快过滤速度,而且能得到比较干燥的晶体.但是,太细的晶体不适合于抽滤.一般情况下,下列哪些因素有利于得到较大的晶体AC.(填写序号)
A.缓慢冷却溶液B.溶质溶解度较小
C.缓慢蒸发溶剂 D.溶液浓度较高
(4)该课题组同学将滤渣1酸浸溶解得到Co2+用盐酸进行溶解.发生如下反应:
2LiCoO2+8HCl═2CoCl2+Cl2+2LiCl+4H2O
在此反应中,体现了盐酸的酸性和还原性.
指导老师建议采用稀硫酸和H2O2溶液溶解,发生如下反应:
2LiCoO2+□+6H++1H2O2=2Co2++1O2↑+2Li++4□
在上述方程式的□中填上缺少的微粒,并进行配平.
你认为指导老师提出该建议的主要依据是用盐酸溶解会产生有毒的氯气污染环境,同时为了除去溶液的Fe2+,还要再加H2O2,操作麻烦
(5)试剂a最好选用下列试剂中的C
A.NaOH溶液 B.(NH4)2CO3溶液 C.NH4HCO3
(6)沉淀2的化学式是Co(OH)2.

已知:金属氢氧化物沉淀的pH值
| 金属氢氧化物 | 金属离子浓度 1mol•L-1 | 金属离子浓度 0.1mol•L-1 | 沉淀完全时的pH值 | |
| 分子式 | Ksp | 开始沉淀时的pH | ||
| Fe(OH)2 | 4.87×10-17 | 5.8 | 6.3 | 8.3 |
| Fe(OH)3 | 2.79×10-39 | 1.2 | 1.5 | 2.8 |
| Co(OH)2 | 5.92×10-15 | 6.9 | 7.4 | 9.4 |
(1)写出钴酸锂正极材料用加5%氢氧化钠溶液,发生的离子反应方程式2Al+2OH-+2H2O=2AlO2-+3H2↑
(2)操作1所用到的玻璃仪器除烧杯、漏斗外,还必须有玻璃棒(填仪器名称).
(3)滤液4到沉淀2可以选择抽滤,抽滤不仅能加快过滤速度,而且能得到比较干燥的晶体.但是,太细的晶体不适合于抽滤.一般情况下,下列哪些因素有利于得到较大的晶体AC.(填写序号)
A.缓慢冷却溶液B.溶质溶解度较小
C.缓慢蒸发溶剂 D.溶液浓度较高
(4)该课题组同学将滤渣1酸浸溶解得到Co2+用盐酸进行溶解.发生如下反应:
2LiCoO2+8HCl═2CoCl2+Cl2+2LiCl+4H2O
在此反应中,体现了盐酸的酸性和还原性.
指导老师建议采用稀硫酸和H2O2溶液溶解,发生如下反应:
2LiCoO2+□+6H++1H2O2=2Co2++1O2↑+2Li++4□
在上述方程式的□中填上缺少的微粒,并进行配平.
你认为指导老师提出该建议的主要依据是用盐酸溶解会产生有毒的氯气污染环境,同时为了除去溶液的Fe2+,还要再加H2O2,操作麻烦
(5)试剂a最好选用下列试剂中的C
A.NaOH溶液 B.(NH4)2CO3溶液 C.NH4HCO3
(6)沉淀2的化学式是Co(OH)2.
13.某溶液可能含有K+、Na+、SO42-、AlO2-、NO3-、I-、Fe2+、Al3+、SiO32-.现进行如下实验:由此可知原溶液中( )
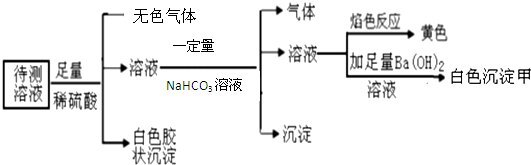

| A. | 一定含有Na+,可能存在K+ | |
| B. | 至少存在4种离子 | |
| C. | 无色气体是NO气体 | |
| D. | 白色沉淀甲中一定含有BaSO4和BaCO3 |
11.下列说法正确的是( )
| A. | 自来水出现水质污染物邻叔丁基苯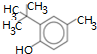 的分子式是C11H16O 的分子式是C11H16O | |
| B. | 有机物CH3CO18OH和C2H5OH在浓硫酸催化作用下产物为CH3CO18OC2H5和H2O | |
| C. | 用乙醇和浓H2SO4制备乙烯时,可用水浴加热控制反应的温度 | |
| D. | 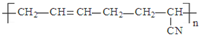 的单体是CH3-C≡C-CH3和CH2=CH-CN 的单体是CH3-C≡C-CH3和CH2=CH-CN |
9.某强酸性溶液X中仅含有NH4+、Al3+、Ba2+、Fe2+、Fe3+、CO32-、SO32-、SO42-、Cl-、NO3-中的一种或几种,取该溶液进行连续实验,实验过程如图: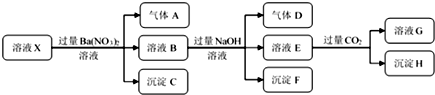
下列有关推断合理的是( )

下列有关推断合理的是( )
| A. | 若要确定溶液X中是否含有Fe3+,其操作为取少量原溶液于试管中,加入适量KSCN溶液,溶液变血红色,则含有Fe3+ | |
| B. | 沉淀C为BaSO4,沉淀H为BaCO3,工业上往BaCO3中加入饱和的Na2CO3可以实现BaSO4的转变 | |
| C. | 溶液中一定含有H+、Al3+、NH4+、Fe2+、SO42-、Cl- | |
| D. | 若溶液X为100 mL,产生的气体A为112 mL(标况),则X中c(Fe2+)=0.05 mol•L-1 |
8.页岩气是蕴藏于页岩层中的天然气,我州页岩气蕴藏量达4.81万亿立方米,约占全省近7成,可采储量超过1.443万亿立方米.页岩气将是我州能源开发的重要方向.下列有关结论中错误的是( )
| A. | 页岩气是一种清洁的能源 | |
| B. | 使用页岩气是对化学能的充分利用 | |
| C. | 使用页岩气给农民的生活带来了不便 | |
| D. | 页岩气是我州解决能源的重要途径 |
7.第ⅦA元素具有相似的化学性质.下列说法中能较好解释这一事实的是( )
0 158016 158024 158030 158034 158040 158042 158046 158052 158054 158060 158066 158070 158072 158076 158082 158084 158090 158094 158096 158100 158102 158106 158108 158110 158111 158112 158114 158115 158116 158118 158120 158124 158126 158130 158132 158136 158142 158144 158150 158154 158156 158160 158166 158172 158174 158180 158184 158186 158192 158196 158202 158210 203614
| A. | 都是非金属元素 | B. | 最外层电子数相同 | ||
| C. | 原子半径相差不大 | D. | 最高化合价相同 |
 .
. .
.
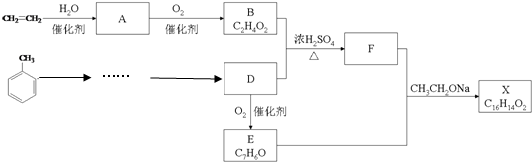
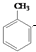 到D的合成路线(无机试剂任选,用合成路线流程图表示).
到D的合成路线(无机试剂任选,用合成路线流程图表示).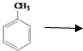
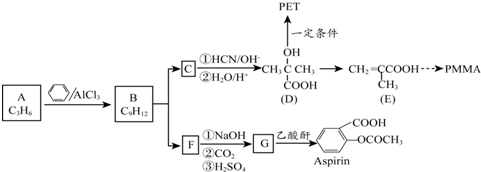
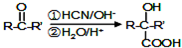
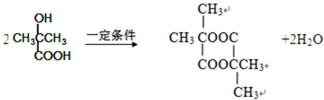 .1mol Aspirin分子与足量的NaOH反应的化学方程式是
.1mol Aspirin分子与足量的NaOH反应的化学方程式是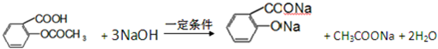 .
.

 .
.