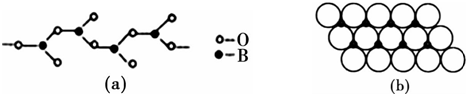3.下列各组物质中,常温下发生反应并放出红棕色气体的是( )
| A. | 铜和浓硫酸 | B. | 铜和浓硝酸 | C. | 铜和浓盐酸 | D. | 铁和稀硫酸 |
2.体积相同的甲、乙两个容器中,分别都充有等物质的量的SO2和O2,在相同温度下发生反应:2SO2(g)+O2(g)?2SO3(g),并达到平衡.在这个过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率( )
| A. | 等于p% | B. | 大于p% | ||
| C. | 小于p% | D. | 达到平衡的时间乙更长 |
1.容积固定为3L的某密闭容器中加入1mol A、2mol B,一定温度下发生如下反应:A(s)+2B(g)?C(g)+D(g),经反应5min后,测得C的浓度为0.3mol•L-1.则下列说法中正确的是( )
| A. | 5 min内D的平均反应速率为0.02 mol•L-1•min-1 | |
| B. | 5 min内A的平均反应速率为0.03 mol•L-1•min-1 | |
| C. | 达平衡后,向容器内再加入少量的A,平衡将向正右移动 | |
| D. | 平衡状态时,生成1molD时同时生成1molA |
19.下列元素中基态原子的第一电离能最大的是( )
| A. | B | B. | C | C. | N | D. | O |
18.检验某溶液中是否含有 K+、Fe3+、Cl-、Mg2+、I-、CO32-、SO42-,限用的试剂有:盐酸、硫酸、硝酸银溶液、硝酸钡溶液.设计如下实验步骤,并记录相关现象.下列叙述不正确的是( )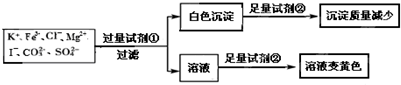

| A. | 试剂①为硝酸钡 | |
| B. | 试剂②一定为盐酸 | |
| C. | 该溶液中一定有 I-、CO32-、SO42-、K+ | |
| D. | 通过在黄色溶液中加入硝酸银溶液可以检验原溶液中是否存在Cl- |
17.地壳中铝元素比铜元素含量高很多,但人们冶炼出铜比铝早很多年.合理的解释是( )
0 158007 158015 158021 158025 158031 158033 158037 158043 158045 158051 158057 158061 158063 158067 158073 158075 158081 158085 158087 158091 158093 158097 158099 158101 158102 158103 158105 158106 158107 158109 158111 158115 158117 158121 158123 158127 158133 158135 158141 158145 158147 158151 158157 158163 158165 158171 158175 158177 158183 158187 158193 158201 203614
| A. | 铜矿颜色较深,易发现;铝矿颜色较浅,不易发现 | |
| B. | 铜矿较易还原,铝矿很难还原 | |
| C. | 矿石在地下埋藏,铜矿最浅,容易开发,铝矿埋得深,难开发 | |
| D. | 铜比铝相对原子质量大 |
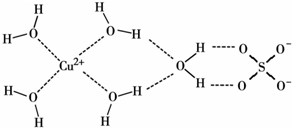
 .
.