8.下列各项操作中,发生“先产生沉淀,然后沉淀又溶解”现象的是( )
①向Ca(ClO)2溶液中通入过量CO2 ②向AlCl3溶液中逐滴加入过量氨水
③向AgNO3溶液中逐滴加入过量氨水 ④向Na2SiO3溶液中逐滴加入过量的盐酸.
①向Ca(ClO)2溶液中通入过量CO2 ②向AlCl3溶液中逐滴加入过量氨水
③向AgNO3溶液中逐滴加入过量氨水 ④向Na2SiO3溶液中逐滴加入过量的盐酸.
| A. | 只有②③ | B. | 只有①③ | C. | 只有①②③ | D. | ①②③④ |
7.(CN)2、(SCN)2、(OCN)2称“类卤素”,与卤素单质的性质相似,而其阴离子性质也相似,如:2Fe+3(SCN)2═2Fe(SCN)3,2Fe+3Cl2═2FeCl3.以此判断下列化学方程式中错误的是( )
| A. | (CN)2+H2O?HCN+HCNO | |
| B. | (SCN)2+2Cu$\frac{\underline{\;\;△\;\;}}{\;}$ 2CuSCN | |
| C. | (OCN)2+2NaOH═NaOCN+NaOCNO+H2O | |
| D. | MnO2+4HSCN(浓)$\frac{\underline{\;\;△\;\;}}{\;}$ (SCN)2↑+Mn(SCN)2+2H2O |
5.下列各表述与示意图一致的是( )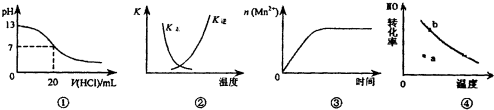

| A. | 图①表示25℃时,用0.1 mol•L-1盐酸滴定20 mL 0,1 mol•L-1 NaOH溶液,溶液的pH随加入酸体积的变化 | |
| B. | 图②中曲线表示反应2SO2(g)+O2(g)?2SO3(g):△H<0正、逆反应的平衡常数K随温度的变化 | |
| C. | 图③表示10 mL 0.01 mol•L-1 KMnO4酸性溶液与过量的0.1 mol•L-1 H2C2O4溶液混合时,n(Mn2+)随时间的变化 | |
| D. | 图④曲线表示2NO+O2?2NO2中NO的最大转化率与温度的关系,a点表示未达到平衡状态,且v(正)<v(逆) |
4.下列实验操作合理的是( )
| A. |  用标准液滴定待测液 | B. |  检查装置气密性 | ||
| C. | 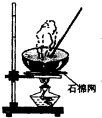 蒸发 | D. |  读取气体体积 |
2.常温下某透明溶液中由水电离出的c(H+)=l×l0-12mol/L,则一定大量共存的离子组是( )
| A. | K+、Fe2+、SO42-、NO3- | B. | Al3+、Na+、HCO-3、Cl- | ||
| C. | Fe3+、K+、Cl-、SCN- | D. | K+、SO2-4,Na+、NO-3 |
1.下列排序错误的是( )
| A. | 熔点:石英>食盐>冰>干冰 | |
| B. | 结合质子(H+)能力:OH->HCO-3>CH3COO- | |
| C. | 离子半径:S2->Cl->Al3+>O2- | |
| D. | 热稳定性:HF>HCl>H2S>PH3 |
20.可逆反应:A+3B?2C+2D(各物质均为气体)在不同情况下测得有下列4 种反应速率,其中反应最快的是( )
| A. | υ( D)=0.4 mol/(L•s) | B. | v( C)=0.8mol/(L•s) | C. | υ( B)=0.6 mol/(L•s) | D. | υ( A)=0.5 mol/(L•s) |
19.利用如图装置可以验证NH3和HCl的有关性质.下列有关说法不正确的是( )
0 158001 158009 158015 158019 158025 158027 158031 158037 158039 158045 158051 158055 158057 158061 158067 158069 158075 158079 158081 158085 158087 158091 158093 158095 158096 158097 158099 158100 158101 158103 158105 158109 158111 158115 158117 158121 158127 158129 158135 158139 158141 158145 158151 158157 158159 158165 158169 158171 158177 158181 158187 158195 203614

| A. | 关闭活塞c,打开活塞a、b,挤压胶头滴管,Ⅱ中产生喷泉 | |
| B. | 关闭活塞a,打开活塞b、c,用热毛巾敷热烧瓶I,I中产生喷泉 | |
| C. | 关闭活塞b,打开活塞a、c,用热毛巾敷热烧瓶II,I中会产生白雾 | |
| D. | 关闭活塞b,打开活塞a、c,用热毛巾敷热烧瓶II,一段时间后,打开活塞b,I、II中均产生喷泉 |
 A、B、C、D、E五种溶液分别是NaOH、NH3•H2O、CH3COOH、HCl、NH4HSO4中的一种.常温下进行下列实验:
A、B、C、D、E五种溶液分别是NaOH、NH3•H2O、CH3COOH、HCl、NH4HSO4中的一种.常温下进行下列实验: