7.下列事实及解释的化学(或离子)方程式均正确的是( )
| A. | MnCl2溶液中常含有Cu2+,可添加难溶电解质MnS除去:Cu2++S2-=CuS↓ | |
| B. | 盛放NaOH溶液的试剂瓶不能用玻璃塞是因为:SiO2+2OH-=SiO32-+H2O | |
| C. | 向FeBr2溶液中通入足量氯气:2Fe2++2Br-+2Cl2═2Fe3++Br2+4Cl- | |
| D. | 向氨水中滴入少量饱和氯化铁溶液制各Fe(OH)3胶体:Fe3++3NH3•H2O?Fe(OH)3(胶体)+3NH4+ |
4.用惰性电极电解一定量的硫酸铜溶液,实验装置如图甲,电解过程中的实验数据如图乙.横坐标表示转移电子的物质的量,纵坐标表示产生气体的总体积(标准状况).则下列说法不正确的是( )

| A. | 电解过程中,a电极表面先有红色物质析出,后有气泡产生 | |
| B. | b电极上发生的反应方程式为:2H2O+2e-═2OH-+H2↑ | |
| C. | 从P到Q点时收集到的混合气体的平均摩尔质量为12 g/mol | |
| D. | 从开始到P点收集到的气体是O2 |
3.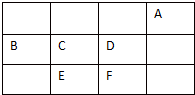 短周期中三元素A、B、C、D、E、F在周期表中的位置如图,下列有关这六种元素的叙述正确的是( )
短周期中三元素A、B、C、D、E、F在周期表中的位置如图,下列有关这六种元素的叙述正确的是( )
 短周期中三元素A、B、C、D、E、F在周期表中的位置如图,下列有关这六种元素的叙述正确的是( )
短周期中三元素A、B、C、D、E、F在周期表中的位置如图,下列有关这六种元素的叙述正确的是( )| A. | E的氢化物的沸点比C的氢化物的沸点低 | |
| B. | F的最高价氧化物的水化物是一种弱酸 | |
| C. | D的氢化物很稳定,因为它含有氢键 | |
| D. | B、C、D原子半径依次递增 |
2.工业上可通过电解NO制备NH4NO3,其工作原理如图所示.下列说法不正确的是( )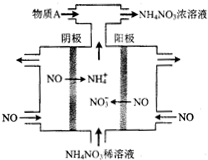

| A. | NO是常见的大气污染物之一,该装置可实现废气的治理与回收利用 | |
| B. | 阳极反应为:NO-3e-+2H2O═NO3-+4H+ | |
| C. | 阴极反应为:NO+5e-+6H+═NH4++H2O | |
| D. | 为使电解产物全部转化为NH4NO3,需向该电解池中补充水 |
20.设NA为阿伏伽德罗常数,下列说法中正确的是( )
| A. | 1molNa2O2固体中含阴离子个数为2NA | |
| B. | 1molSiO2中含Si-O的数目为2NA | |
| C. | 标准状况下,22.4L乙炔中含π键数为2NA | |
| D. | 1molNaHCO3晶体中阳离子数为2NA |
19.下列说法正确的是( )
0 157999 158007 158013 158017 158023 158025 158029 158035 158037 158043 158049 158053 158055 158059 158065 158067 158073 158077 158079 158083 158085 158089 158091 158093 158094 158095 158097 158098 158099 158101 158103 158107 158109 158113 158115 158119 158125 158127 158133 158137 158139 158143 158149 158155 158157 158163 158167 158169 158175 158179 158185 158193 203614
| A. | 硒化氢(H2Se)是有色、有毒的气体,比H2S稳定 | |
| B. | Na2O2中阳离子与阴离子的个数比为1:1 | |
| C. | Ba(OH)2•8H2O晶体与氯化铵晶体反应不需要加热就能发生,说明该反应是放热反应 | |
| D. | 由H2→2H的过程需要吸收能量 |
 (1)为了做到合理营养,我国营养学家将食物分为A、B、C、D、E五类,请回答下列问题:①营养学家将这五类形象地设计成图示的“平衡膳食宝塔”,并提倡居民每天均衡地吃这五类食物.为保证身体健康,建议在每日摄入的总能量中,早、中、晚餐的能量比例是3:4:3.
(1)为了做到合理营养,我国营养学家将食物分为A、B、C、D、E五类,请回答下列问题:①营养学家将这五类形象地设计成图示的“平衡膳食宝塔”,并提倡居民每天均衡地吃这五类食物.为保证身体健康,建议在每日摄入的总能量中,早、中、晚餐的能量比例是3:4:3.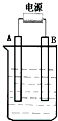 在如图用石墨作电极的电解池中,放入500mL含一种溶质的某蓝色溶液进行电解,观察到A电极表面有红色的固态物质生成,B电极有无色气体生成;当溶液中的原有溶质完全电解后,停止电解,取出A电极,洗涤、干燥、称量、电极增重1.6g.请回答下列问题:
在如图用石墨作电极的电解池中,放入500mL含一种溶质的某蓝色溶液进行电解,观察到A电极表面有红色的固态物质生成,B电极有无色气体生成;当溶液中的原有溶质完全电解后,停止电解,取出A电极,洗涤、干燥、称量、电极增重1.6g.请回答下列问题: