6.将1mol碳在氧气中完全燃烧生成气体,放出393kJ的热量,下列热化学方程式表示正确的是( )
| A. | C(s)+O2(g)→CO2(g)+393kJ | B. | C+O2→CO2+393kJ | ||
| C. | C(s)+O2(g)→CO2(g)-393kJ | D. | C(s)+1/2O2(g)→CO(g)+393kJ |
4.下列图示与对应的叙述正确的是( )
| A. | 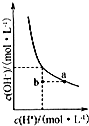 如图为在水溶液中H+和OH-的浓度变化曲线,恒温稀释可实现a→b的转化 | |
| B. |  如图为H2O2在有、无催化剂下的分解反应曲线b表示有催化剂时的反应 | |
| C. | 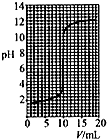 如图可表示用0.0110mol/L盐酸滴定0.0110mol/L氨水时的滴定曲线 | |
| D. | 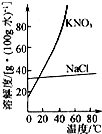 如图为NaCl中含有少量KNO3,可在较高温度下制得浓溶液再冷却结晶、过滤、干燥 |
3.室温下,0.1mol/L的H2A溶液体系中,含A粒子的分布系数(平衡时某粒子的浓度占各粒子浓度之和的分数)与溶液 pH的关系如图所示.下列说法不正确的是( )

0 157985 157993 157999 158003 158009 158011 158015 158021 158023 158029 158035 158039 158041 158045 158051 158053 158059 158063 158065 158069 158071 158075 158077 158079 158080 158081 158083 158084 158085 158087 158089 158093 158095 158099 158101 158105 158111 158113 158119 158123 158125 158129 158135 158141 158143 158149 158153 158155 158161 158165 158171 158179 203614

| A. | 室温下,HA-的电离常数Ka2=1.0×10-7 | |
| B. | 室温下,0.1mol/L的NaHA溶液显酸性 | |
| C. | 室温下,0.2mol/L的H2A与0.1mol/L的NaOH溶液等体积混合,溶液pH=1.8 | |
| D. | 0.1mol/L的Na2A溶液中c(OH-)=c(H+)+c(HA-)+2c(H2A) |
 (或
(或 ).
).
 氯化铁是实验室中的重要试剂.某同学用m g含有铁锈(Fe2O3)的废铁屑来制取FeCl3•6H2O晶体,同时测定废铁屑中铁的质量分数,为此设计了如下装置(夹持装置略,气密性已检验):
氯化铁是实验室中的重要试剂.某同学用m g含有铁锈(Fe2O3)的废铁屑来制取FeCl3•6H2O晶体,同时测定废铁屑中铁的质量分数,为此设计了如下装置(夹持装置略,气密性已检验):
