18.下列化合物中,就有离子键,又有共价键的是( )
| A. | H2O | B. | CaCl2 | C. | KOH | D. | NH3 |
16.A、B、C三种元素的原子序数依次为a、b、c,它们的离子An+、Bm-、Cn-具有相同的电子层结构,且n>m,则下列关系正确的是( )
| A. | a>b>c | B. | a>c>b | C. | a=b+m+n | D. | a=c-n-m |
12.A、B、C、D、E是同一周期的五种主族元素,A和B的最高价氧化物对应的水化物均呈碱性,且碱性B>A,C和D的气态氢化物的稳定性C>D;E是这五种元素中离子半径最小的元素,则它们的原子序数由小到大的顺序是( )?
| A. | A、B、C、D、E | B. | B、A、E、D、C | C. | B、A、D、C、E | D. | C、D、A、B、E |
11.某无色透明呈强碱性溶液中能大量共存的离子组是( )
| A. | Na+ Cu2+ NO3- Cl- | B. | K+ NO3- Na+ Cl- | ||
| C. | K+ CO32- NO3- Ca2+ | D. | K+ NO3- SO42- Mg2+ |
9.运用化学反应原理研究卤族元素的性质具有重要意义.
(1)下列关于氯水的叙述正确的是aef(填写符号).
a.氯水中存在两种电离平衡
b.向氯水中通入SO2,其漂白性增强
c.向氯水中通入氯气,c(H+)/c(ClO-)减小
d.加水稀释氯水,溶液中的所有离子浓度均减小
e.加水稀释氯水,水的电离平衡向正反应方向移动
f.向氯水中加入少量固体NaOH,可能有c(Na+)=c(Cl-)+c(ClO-)
(2)常温下,已知25℃时有关弱酸的电离平衡离数:
写出84消毒液露置在空气中发生反应的离子方程式ClO-+CO2+H2O═HClO+HCO3-2HClO $\frac{\underline{\;光照\;}}{\;}$2H++2Cl-+O2↑.
(3)电解饱和食盐水可得到溶质为M的碱溶液,常温下将浓度为c1的M溶液与0.1mol•L-1的一元酸HA等体积混合,所得溶液pH=7,则c1≤ 0.1mol•L-1(填“≥”、“≤”或“=”),溶液中离子浓度的大小关系为c(Na+)=c(A-)>c(OH-)=c(H+).若将上述“0.1mol•L-1的一元酸HA”改为“pH=1的一元酸HA”,所得溶液的pH仍为7,则c1≥0.1mol•L-1.
(4)牙釉质对牙齿起着保护作用,其主要成分为羟基磷灰石(Ca5(PO4)3OH),研究证实氟磷灰石(Ca5(PO4)3F)比它更能抵抗酸的侵蚀,故含氟牙膏已使全世界千百万人较少龋齿,请写出羟基磷灰石的溶度积常数表达式Ksp=c5(Ca2+)c3(PO43-)c(OH-),氟离子与之反应转化的离子方程式为Ca5(PO4)3OH+F-═Ca5(PO4)3F+OH-.
0 157977 157985 157991 157995 158001 158003 158007 158013 158015 158021 158027 158031 158033 158037 158043 158045 158051 158055 158057 158061 158063 158067 158069 158071 158072 158073 158075 158076 158077 158079 158081 158085 158087 158091 158093 158097 158103 158105 158111 158115 158117 158121 158127 158133 158135 158141 158145 158147 158153 158157 158163 158171 203614
(1)下列关于氯水的叙述正确的是aef(填写符号).
a.氯水中存在两种电离平衡
b.向氯水中通入SO2,其漂白性增强
c.向氯水中通入氯气,c(H+)/c(ClO-)减小
d.加水稀释氯水,溶液中的所有离子浓度均减小
e.加水稀释氯水,水的电离平衡向正反应方向移动
f.向氯水中加入少量固体NaOH,可能有c(Na+)=c(Cl-)+c(ClO-)
(2)常温下,已知25℃时有关弱酸的电离平衡离数:
| 弱酸化学式 | HClO | H2CO3 |
| 电离平衡常数 | 4.7×10-8 | K1=4.3×10-7 K2=5.6×10-11 |
(3)电解饱和食盐水可得到溶质为M的碱溶液,常温下将浓度为c1的M溶液与0.1mol•L-1的一元酸HA等体积混合,所得溶液pH=7,则c1≤ 0.1mol•L-1(填“≥”、“≤”或“=”),溶液中离子浓度的大小关系为c(Na+)=c(A-)>c(OH-)=c(H+).若将上述“0.1mol•L-1的一元酸HA”改为“pH=1的一元酸HA”,所得溶液的pH仍为7,则c1≥0.1mol•L-1.
(4)牙釉质对牙齿起着保护作用,其主要成分为羟基磷灰石(Ca5(PO4)3OH),研究证实氟磷灰石(Ca5(PO4)3F)比它更能抵抗酸的侵蚀,故含氟牙膏已使全世界千百万人较少龋齿,请写出羟基磷灰石的溶度积常数表达式Ksp=c5(Ca2+)c3(PO43-)c(OH-),氟离子与之反应转化的离子方程式为Ca5(PO4)3OH+F-═Ca5(PO4)3F+OH-.
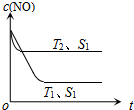 汽车尾气是城市的主要空气污染物,研究控制汽车尾气成为保护环境的首要任务.
汽车尾气是城市的主要空气污染物,研究控制汽车尾气成为保护环境的首要任务.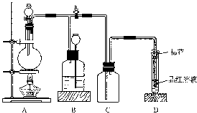 如图所示装置为铜跟浓硫酸反应制取二氧化硫的实验装置:
如图所示装置为铜跟浓硫酸反应制取二氧化硫的实验装置: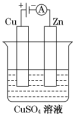 (1)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料.已知在100kPa时,32.0g N2H4在氧气中完全燃烧生成氮气,放出热量624kJ(25℃),N2H4完全燃烧的热化学方程式是N2H4(l)+2H2O2(l)=N2(g)+4H2O(l)△H=-642kJ/mol.
(1)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料.已知在100kPa时,32.0g N2H4在氧气中完全燃烧生成氮气,放出热量624kJ(25℃),N2H4完全燃烧的热化学方程式是N2H4(l)+2H2O2(l)=N2(g)+4H2O(l)△H=-642kJ/mol.