18.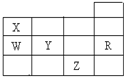 如图所示为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( )
如图所示为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( )
 如图所示为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( )
如图所示为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( )| A. | 元素原子半径:W<Y | |
| B. | X、Y的阴离子电子层结构都与R原子相同 | |
| C. | Y元素的非金属性比W元素的非金属性强 | |
| D. | 常温常压下五种元素的单质中,Z单质的沸点最高 |
16.在盛有少量氯水的试管中加入过量的溴化钾溶液,再加入少量四氯化碳,振荡静置后可观察到的现象是( )
| A. | 溶液呈橙色不分层 | B. | 溶液分两层,上层呈橙色 | ||
| C. | 溶液分两层,下层呈橙色 | D. | 溶液呈紫色不分层 |
15.决定核素种类的是( )
| A. | 质子数 | B. | 中子数 | ||
| C. | 原子的最外层电子数 | D. | 质子数和中子数 |
14.如图是实验室制取氨气的装置和选用的试剂,其中错误的是( )
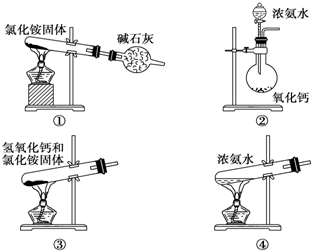

| A. | ①② | B. | ①③ | C. | ②③ | D. | ②④ |
12.下列化学反应的离子方程式正确的是( )
| A. | 在稀氨水中通入过量CO2:NH3•H2O+CO2═NH4++HCO3- | |
| B. | 铁与稀HNO3反应:Fe+2H+=═Fe2++H2↑ | |
| C. | 用稀HNO3溶解FeS固体:FeS+2H+═Fe2++H2S↑ | |
| D. | 将氯化亚铁溶液和稀硝酸混合:Fe2++4H++NO3-═Fe3++2H20+NO↑ |
11.下列现象与氢键有关的是( )
①HF的熔、沸点比HCl的熔、沸点高②NH3极易溶于水③冰的密度比液态水的密度小④水分子高温下很稳定.
①HF的熔、沸点比HCl的熔、沸点高②NH3极易溶于水③冰的密度比液态水的密度小④水分子高温下很稳定.
| A. | ①②③④ | B. | ①②③ | C. | ①② | D. | ①③ |
10.铵盐是一类重要的氮的化合物,设NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 0.1 mol NH4+含有的电子数为1.1NA | |
| B. | NH4+中N元素的化合价为-3,在氧化还原反应中常作氧化剂 | |
| C. | 0.1 L 3 mol•L-1的NH4NO3溶液中氮原子数等于0.6NA | |
| D. | 5NH4NO3$\frac{\underline{\;\;△\;\;}}{\;}$2HNO3+4N2↑+9H2O反应中,生成56gN2时,转移的电子数目为3.75NA |
9.在汽车排气管加装催化装置,可有效减少CO和NOx的排放,催化装置内发生反应为NOx+CO$\stackrel{催化剂}{→}$N2+CO2(未配平),下列关于此反应的说法中错误的是( )
0 157971 157979 157985 157989 157995 157997 158001 158007 158009 158015 158021 158025 158027 158031 158037 158039 158045 158049 158051 158055 158057 158061 158063 158065 158066 158067 158069 158070 158071 158073 158075 158079 158081 158085 158087 158091 158097 158099 158105 158109 158111 158115 158121 158127 158129 158135 158139 158141 158147 158151 158157 158165 203614
| A. | 该反应中化合价变化的有N、C元素 | |
| B. | 当x=2时,每生成1 mol N2,转移电子数为4 mol | |
| C. | 等物质的量N2和CO2中,共价键的个数比为3:4 | |
| D. | 氧化剂与还原剂的物质的量之比为1:2时,NOx中氮元素的化合价为+4价 |