10.下列关于化学键的说法,正确的是( )
| A. | 构成单质的分子中一定含有共价键 | |
| B. | 由非金属元素组成的化合物可能是离子化合物 | |
| C. | 非极性键只存在单质分子里 | |
| D. | 不同元素组成的多原子分子里的化学键一定是极性键 |
9.25°C时,将两铜电极插入一定量的饱和硫酸钠溶液中进行电解,通电一段时间后,阴极出现了amol气体,同时有W gNa2SO4•10H2O晶体析出,温度不变时剩余溶液中溶质的质量分数为( )
| A. | $\frac{71ω}{161(ω+α)}$×100% | B. | $\frac{71ω}{161(ω+18α)}$×100% | ||
| C. | $\frac{ω}{ω+18α}$×100% | D. | $\frac{ω}{ω+36α}$×100% |
8.下列叙述正确的是( )
①锌跟稀硫酸反应制取氢气,加入少量硫酸铜溶液能加快反应速率
②镀层破损后,白铁(镀锌的铁)比马口铁(镀锡的铁)更易腐蚀
③电镀时,应把待镀金属置于电解槽的阴极
④电解饱和氯化钠溶液可以冶炼出金属钠
⑤钢铁表面常易锈蚀生成Fe2O3•nH2O
⑥粗铜精炼时粗铜连接电源的正极
⑦金属的防护中,牺牲阳极的阴极保护法是让被保护金属做原电池的负极.
①锌跟稀硫酸反应制取氢气,加入少量硫酸铜溶液能加快反应速率
②镀层破损后,白铁(镀锌的铁)比马口铁(镀锡的铁)更易腐蚀
③电镀时,应把待镀金属置于电解槽的阴极
④电解饱和氯化钠溶液可以冶炼出金属钠
⑤钢铁表面常易锈蚀生成Fe2O3•nH2O
⑥粗铜精炼时粗铜连接电源的正极
⑦金属的防护中,牺牲阳极的阴极保护法是让被保护金属做原电池的负极.
| A. | ①②③⑤⑥⑦ | B. | ①③⑤⑦ | C. | ①③⑤⑥ | D. | ①②③⑥⑦ |
7.铊是超导材料的组成元素之一,铊位于第六周期ⅢA族,元素符号是Tl.以下对铊的性质推断中肯定不正确的是( )
| A. | 铊是易导电的银白色金属 | B. | 能生成+3价的离子化合物 | ||
| C. | 能与H+反应生成H2 | D. | Tl3+的氧化性比Al3+强 |
3. 已知:常温下,(1)Ka1(H2CO3)=4.3×10-7,Ka2(H2CO3)=5.6×10-11;(2)H2R及其钠盐的溶液中,H2R、HR-、R2-分别在三者中所占的物质的量分数(α)随溶液pH变化关系如图所示,下列叙述错误的是( )
已知:常温下,(1)Ka1(H2CO3)=4.3×10-7,Ka2(H2CO3)=5.6×10-11;(2)H2R及其钠盐的溶液中,H2R、HR-、R2-分别在三者中所占的物质的量分数(α)随溶液pH变化关系如图所示,下列叙述错误的是( )
 已知:常温下,(1)Ka1(H2CO3)=4.3×10-7,Ka2(H2CO3)=5.6×10-11;(2)H2R及其钠盐的溶液中,H2R、HR-、R2-分别在三者中所占的物质的量分数(α)随溶液pH变化关系如图所示,下列叙述错误的是( )
已知:常温下,(1)Ka1(H2CO3)=4.3×10-7,Ka2(H2CO3)=5.6×10-11;(2)H2R及其钠盐的溶液中,H2R、HR-、R2-分别在三者中所占的物质的量分数(α)随溶液pH变化关系如图所示,下列叙述错误的是( )| A. | 在pH=4.3的溶液中:3c(R2-)=c(Na+)+c(H+)-c(OH-) | |
| B. | 等体积等浓度的NaOH溶液与H2R溶液混合后,溶液中水的电离程度比纯水小 | |
| C. | 在pH=3的溶液中存在$\frac{c({R}^{2-})×c({H}_{2}R)}{c(H{R}^{-})}$=10-3 | |
| D. | 向Na2CO3溶液中加入少量H2R溶液,发生反应:CO32-+H2R=HCO3-+HR- |
1.A、B、C、D、E、F是中学化学中常见的六种短周期元素,有关位置及信息如下:A的气态氢化物水溶液呈碱性;C单质一般保存在煤油中;F的最高价氧化物对应的水化物既能与酸反应又能与碱反应,G单质是日常生活中用量最大的金属,易被腐蚀或损坏.请回答下列问题:
(1)A的最高价氧化物对应的水化物与其氢化物反应生成离子化合物的化学式为NH4NO3.
(2)由C、B、F三种元素构成的化合物中含有的化学键类型共价键和离子键
(3)A与B可组成质量比为7:16的三原子分子,该分子释放在空气中其化学作用可能引发的后果有①③(填序号).
①酸雨 ②温室效应 ③光化学烟雾 ④臭氧层破坏
(4)若在D与G组成的某种化合物的溶液甲中,加入铜片,溶液会慢慢变为蓝色,依据产生该现象的反应原理,可设计成的原电池,则其正极反应式为2Fe3++2e-=2Fe2+.
0 157940 157948 157954 157958 157964 157966 157970 157976 157978 157984 157990 157994 157996 158000 158006 158008 158014 158018 158020 158024 158026 158030 158032 158034 158035 158036 158038 158039 158040 158042 158044 158048 158050 158054 158056 158060 158066 158068 158074 158078 158080 158084 158090 158096 158098 158104 158108 158110 158116 158120 158126 158134 203614
| … | E | A | B | ||
| C | … | D |
(2)由C、B、F三种元素构成的化合物中含有的化学键类型共价键和离子键
(3)A与B可组成质量比为7:16的三原子分子,该分子释放在空气中其化学作用可能引发的后果有①③(填序号).
①酸雨 ②温室效应 ③光化学烟雾 ④臭氧层破坏
(4)若在D与G组成的某种化合物的溶液甲中,加入铜片,溶液会慢慢变为蓝色,依据产生该现象的反应原理,可设计成的原电池,则其正极反应式为2Fe3++2e-=2Fe2+.
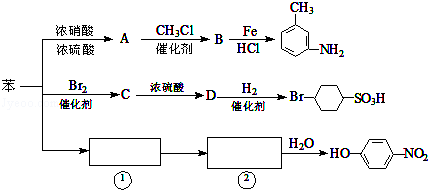
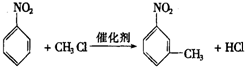 .
.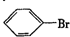 ,②
,②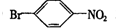 .
.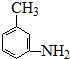 的所有原子不是(填“是”或“不是”)在同一平面上.
的所有原子不是(填“是”或“不是”)在同一平面上.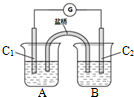 已知砷(As)元素的原子结构示意图为:
已知砷(As)元素的原子结构示意图为:


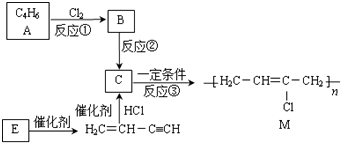
 ,该反应类型属于消去反应.
,该反应类型属于消去反应. .
.