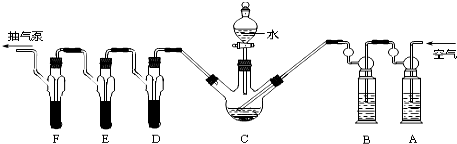
11.类比法是化学学习和研究中常用的重要思维方法,但所得结论要经过实践的检验才能确定其正确与否.根据你所掌握的知识,判断下列类推结论中正确的是( )
| 化学事实 | 类推结论 | |
| A | pH=3盐酸稀释1000倍后pH=6 | pH=6盐酸稀释1000倍后pH=9 |
| B | 用电解熔融MgCl2制取金属Mg | 用电解熔融NaCl冶炼金属钠 |
| C | Na着火不能用干冰灭火 | K着火不能用干冰灭火 |
| D | 将SO2通入BaCl2溶液无沉淀生成 | 将SO2通入Ba(NO3)2溶液也无沉淀生成 |
| A. | A | B. | B | C. | C | D. | D |
10.下列有关化学用语使用正确的是( )
| A. | 质量数为37的氯原子:${\;}_{37}^{17}$Cl | |
| B. | 次氯酸分子的电子式: | |
| C. | 乙酸乙酯的结构简式: | |
| D. | Al(OH)3的电离:H++AlO2-+H2O?Al(OH)2?Al3++3OH- |
9.下述实验不能达到预期目的是( )
| 实验内容 | 实验目的 | |
| A | 将AlCl3溶液蒸干灼烧 | 制备Al2O3 |
| B | 向淀粉水解后的溶液中,依次加入NaOH溶液、新制Cu(OH)2,共热 | 探究水解产物的还原性 |
| C | 向某溶液中加入稀硫酸,将产生的气体通入澄清石灰水 | 检验该溶液中是否含有CO32- |
| D | 向H2O2溶液中滴加少量FeCl3溶液 | 探究催化剂对化学反应速率的影响 |
| A. | A | B. | B | C. | C | D. | D |
7.NA表示阿伏伽德罗常数,下列说法正确的是( )
| A. | 标准状况下,11.2L的水中含有0.5NA个水分子 | |
| B. | 含有1molHCl的盐酸中离子总数为NA个 | |
| C. | 1molO2和H2的混合气体中含有NA个分子 | |
| D. | 1mol大米中含有NA个大米粒子 |
5.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 10 g 46%的乙醇水溶液中所含氢原子数目为1.2NA | |
| B. | 标准状况下,2.24 L氯气溶于水发生反应,转移的电子数目为0.1NA | |
| C. | 高温下,0.2 mol的铁与足量的水蒸气反应,生成氢气的分子数目为0.3NA | |
| D. | 25℃时,100 mL pH=13的Ba(OH)2溶液中OH-的数目为0.02NA |
4.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 将1 mol Cl2通入到水中,则N(HClO)+N(Cl-)+N(ClO-)=2NA | |
| B. | 常温常压下,3.0 g含甲醛的冰醋酸中含有的原子总数为0.4NA | |
| C. | 标准状况下,2.24 L的CCl4中含有的C-Cl键数为0.4NA | |
| D. | 将CO2通过Na2O2使其增重a克时,反应中转移的电子数为NA |
3.过氧化钙(CaO2)是一种白色结晶体粉末,极微溶于水,不溶于醇类、乙醚等,加热至350℃左右开始分解放出氧气,与水缓慢反应生成H2O2.易于酸反应生成H2O2,过氧化钙可用于改善水质、处理含重金属粒子废水和治理赤潮,也可用于应急供氧等,是一种重要化工试剂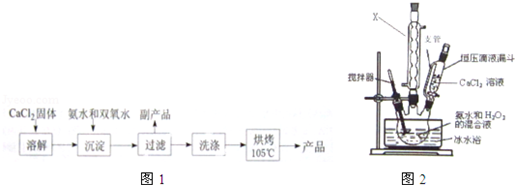
(Ⅰ)CaO2的制备原理:CaCl2+H2O2+2NH3•H2O+6H2O═CaO2•8H2O↓+2NH4Cl实验步骤如图1,反应装置如图2所示,请回答下列问题:
(1)X仪器名称球形冷凝管.
(2)加入氨水的作用是中和反应生成的HCl,使CaCl2+H2O2?CaO2+2HCl向右进行.
(3)沉淀反应时常用冰水浴控制温度在0℃左右,其可能原因是减少双氧水受热分解、降低产物溶解度便于析出(或该反应放热)(写出两种)
(4)过滤后洗涤沉淀的试剂最好用B
A.热水B.冷水C.乙醇D.乙醚
(5)CaO2贮存时应该注意的问题是密封(或防潮、避免与易燃物接触等)(写一条即可)
(Ⅱ)CaO2纯度检测,将一定量CaO2溶于稀硫酸,用标准KMnO4溶于滴定生成的H2O2(KMnO4反应后生成Mn2+)计算确定CaO2的含量.
(6)现每次称取0.4000g样品溶解后,用0.1000mol/L的KMnO4溶液滴定所得数据如表所示,则CaO2样品的纯度90.00%
(7)测得CaO2样品纯度偏低的原因可能是AD
A.烘烤时间不足
B.在洁净干燥的酸式滴定管中未润洗即装标准液
C.滴定前尖嘴处有气泡.滴定后消失
D.配置KMnO4标准溶液定容时俯视容量瓶标线.
0 157933 157941 157947 157951 157957 157959 157963 157969 157971 157977 157983 157987 157989 157993 157999 158001 158007 158011 158013 158017 158019 158023 158025 158027 158028 158029 158031 158032 158033 158035 158037 158041 158043 158047 158049 158053 158059 158061 158067 158071 158073 158077 158083 158089 158091 158097 158101 158103 158109 158113 158119 158127 203614

(Ⅰ)CaO2的制备原理:CaCl2+H2O2+2NH3•H2O+6H2O═CaO2•8H2O↓+2NH4Cl实验步骤如图1,反应装置如图2所示,请回答下列问题:
(1)X仪器名称球形冷凝管.
(2)加入氨水的作用是中和反应生成的HCl,使CaCl2+H2O2?CaO2+2HCl向右进行.
(3)沉淀反应时常用冰水浴控制温度在0℃左右,其可能原因是减少双氧水受热分解、降低产物溶解度便于析出(或该反应放热)(写出两种)
(4)过滤后洗涤沉淀的试剂最好用B
A.热水B.冷水C.乙醇D.乙醚
(5)CaO2贮存时应该注意的问题是密封(或防潮、避免与易燃物接触等)(写一条即可)
(Ⅱ)CaO2纯度检测,将一定量CaO2溶于稀硫酸,用标准KMnO4溶于滴定生成的H2O2(KMnO4反应后生成Mn2+)计算确定CaO2的含量.
(6)现每次称取0.4000g样品溶解后,用0.1000mol/L的KMnO4溶液滴定所得数据如表所示,则CaO2样品的纯度90.00%
| 实验序号 | 第1次 | 第2次 | 第3次 | 第4次 |
| 消耗KMnO4体积/mL | 19.98 | 20.02 | 20.20 | 20.00 |
A.烘烤时间不足
B.在洁净干燥的酸式滴定管中未润洗即装标准液
C.滴定前尖嘴处有气泡.滴定后消失
D.配置KMnO4标准溶液定容时俯视容量瓶标线.
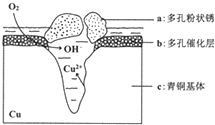 我国古代青铜器工艺精湛,有很高的艺术价值和历史价值,但出土的青铜器因受到环境腐蚀,欲对其进行修复和防护具有重要意义.
我国古代青铜器工艺精湛,有很高的艺术价值和历史价值,但出土的青铜器因受到环境腐蚀,欲对其进行修复和防护具有重要意义.