2.下列说法正确的是( )
| A. | 酸碱中和滴定到终点读数时,发现滴定管尖嘴处悬挂一滴溶液,导致实验结果偏高 | |
| B. | 某溶液中滴加HNO3无明显现象,再滴加Ba(NO3)2溶液出现白色沉淀,说明原溶液中含有SO42- | |
| C. | 制备乙酸乙酯的实验中,用饱和食盐水除杂 | |
| D. | 在蒸发皿中加热蒸干AlCl3可以得到该物质的固体 |
1.下列说法不正确的是( )
| A. | 通过红外光谱分析可以区分乙醇和乙酸 | |
| B. | 可用蘸浓盐酸的棉棒检验输送氨气的管道是否漏气 | |
| C. | 光催化还原水制氢比电解水制氢更节能环保、更经济 | |
| D. | 石油的裂解、煤的干馏、蛋白质的盐析和淀粉的水解都是化学变化 |
20.下列说法正确的是( )
| A. | 正戊烷、异戊烷和新戊烷互为同分异构体,沸点依次升高 | |
| B. | 乙醇依次通过消去、取代、加成反应可生成乙二醇 | |
| C. | 在鸡蛋清溶液中分别加入饱和Na2SO4、CuSO4溶液,都会因盐析产生沉淀 | |
| D. | 等质量的甲烷、乙烯、1,3-丁二烯分别充分燃烧,所耗用氧气的量依次减少 |
19.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 235g的${\;}_{92}^{235}U$发生裂变反应:${\;}_{92}^{235}$U+${\;}_0^1$n$\stackrel{裂变}{→}$${\;}_{38}^{90}$Sr+${\;}_{54}^{136}$U+10${\;}_0^1$n,净产生的中子(${\;}_0^1$n)数为10NA | |
| B. | 12g石墨烯(单层石墨)中含有六元环的个数为NA | |
| C. | 常温常压下,14g由N2与CO组成的混合气体含有的原子数目为NA | |
| D. | 标准状况下,6.72L NO2与水充分反应转移的电子数目为0.1NA |
18.化学与生产、生活、环境保护等密切相关,下列叙述正确的是( )
| A. | 明矾溶于水会形成胶体,因此可用于自来水的杀菌消毒 | |
| B. | 新型材料聚酯纤维、光导纤维都属于有机高分子材料 | |
| C. | 医药中常用95%酒精来消毒,是因为酒精能够使病毒的蛋白质发生变性 | |
| D. | 常压下,0℃时冰的密度比水的密度小,水在4℃时密度最大,这些都与分子间的氢键有关 |
17.某化学探究小组拟用废铜屑制取Cu(NO3)2,并探究其化学性质.
I.如图1,用浓HNO3,和过量的废铜屑充分反应制硝酸铜溶液.
(1)写出铜与浓硝酸反应的离子方程式Cu+4H++2NO3-=Cu2++2NO2↑+2H2O.
(2)①装置中NaOH溶液的作用是吸收氮氧化物,防止污染空气.
②欲从反应后的溶液中得到硝酸铜晶体,实验操作步骤是蒸发浓缩、冷却结晶、过滤.
③你认为此装置是否合理,并说明原因不合理,密闭体系中立即产生大量气体,会有安全隐患;或者合理,慢慢挤压,胶头滴管控制反应速率,使NaOH溶液及时吸收NO2.
如果不合理,同时在原装置上改进;如果合理,只需说明原因.
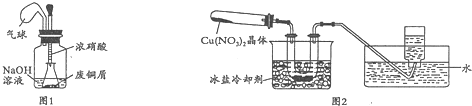
Ⅱ.为了探究Cu(NO3)2的热稳定性,探究小组按图2装置进行实验.(图中铁架台、铁夹和加热仪器均略去)
【实验装置】
【实验操作及现象】往试管中放入研细的无水Cu(NO3)2晶体并加热,观察到试管中有红棕色气体生成,最终残留黑色粉末;用U型管除去红棕色气体,在集气瓶中收集到无色气体.
【解释与结论】
(3)①红棕色气体是NO2.
②根据现象判断Cu(NO3)2在加热条件下可以分解,其化学反应方程式为2Cu(NO3)2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+4NO2↑+O2↑.
Ⅲ.利用Cu(NO3)2制备浅绿色的碱式碳酸铜[CuCO3•Cu(OH)2].
向大试管中加入一定量的碳酸钠溶液和硝酸铜溶液,水浴加热,用0.4mol•L-1的NaOH溶液调节pH至8.5,振荡、静置、过滤、洗涤、干燥,得到样品.
【实验数据】反应温度对样品的影响
(4)滤液中可能含有CO32-,写出检验CO32-的方法取少量滤液置于试管中,加入足量稀盐酸,将产生的气体通入澄清石灰水,溶液变浑浊,说明含碳酸根离子.
(5)95℃时,样品颜色发暗的原因:含有黑色的氧化铜.
(6)70℃时,实验得到2.38g样品,取此样品加热至分解完全(杂质不分解),得到1.76g固体,此样品中碱式碳酸铜的质量分数是93.3%.
I.如图1,用浓HNO3,和过量的废铜屑充分反应制硝酸铜溶液.
(1)写出铜与浓硝酸反应的离子方程式Cu+4H++2NO3-=Cu2++2NO2↑+2H2O.
(2)①装置中NaOH溶液的作用是吸收氮氧化物,防止污染空气.
②欲从反应后的溶液中得到硝酸铜晶体,实验操作步骤是蒸发浓缩、冷却结晶、过滤.
③你认为此装置是否合理,并说明原因不合理,密闭体系中立即产生大量气体,会有安全隐患;或者合理,慢慢挤压,胶头滴管控制反应速率,使NaOH溶液及时吸收NO2.
如果不合理,同时在原装置上改进;如果合理,只需说明原因.

Ⅱ.为了探究Cu(NO3)2的热稳定性,探究小组按图2装置进行实验.(图中铁架台、铁夹和加热仪器均略去)
【实验装置】
【实验操作及现象】往试管中放入研细的无水Cu(NO3)2晶体并加热,观察到试管中有红棕色气体生成,最终残留黑色粉末;用U型管除去红棕色气体,在集气瓶中收集到无色气体.
【解释与结论】
(3)①红棕色气体是NO2.
②根据现象判断Cu(NO3)2在加热条件下可以分解,其化学反应方程式为2Cu(NO3)2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+4NO2↑+O2↑.
Ⅲ.利用Cu(NO3)2制备浅绿色的碱式碳酸铜[CuCO3•Cu(OH)2].
向大试管中加入一定量的碳酸钠溶液和硝酸铜溶液,水浴加热,用0.4mol•L-1的NaOH溶液调节pH至8.5,振荡、静置、过滤、洗涤、干燥,得到样品.
【实验数据】反应温度对样品的影响
| 实验序号 | 1 | 2 | 3 | 4 |
| 温度/℃ | 35 | 50 | 70 | 95 |
| 样品颜色 | 深蓝色 | 深蓝色 | 浅绿色 | 暗蓝色 |
| 样品中碱式碳酸铜的质量分数/% | 90.9 | 92.7 | x | 92.0 |
(5)95℃时,样品颜色发暗的原因:含有黑色的氧化铜.
(6)70℃时,实验得到2.38g样品,取此样品加热至分解完全(杂质不分解),得到1.76g固体,此样品中碱式碳酸铜的质量分数是93.3%.
16.设NA表示阿伏加德罗常数,下列叙述正确的是( )
| A. | 1L 0.1mol•L-1的氨水含有0.1 NA个OH- | |
| B. | 常温常压下的33.6L氯气与27g铝充分反应,转移电子数为3NA | |
| C. | 80℃时,1L pH=1的硫酸溶液中,含有0.2NA个H+ | |
| D. | 在电解精炼粗铜的过程中,当阴极析出32g铜时转移电子数为NA |
15.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 标准状况下,5.6L NO和5.6L O2混合后的分子总数为0.5NA | |
| B. | 25g 质量分数为68%的H2O2水溶液中含氧原子数目为NA | |
| C. | 高温下,16.8g Fe 与足量水蒸气完全反应失去0.8NA个电子 | |
| D. | 1mol CH5+中含有的电子数目为11NA |
14.《本草纲目》卷七记载“石碱条”:“彼人采蒿蓼之属,晒干烧灰,以水淋汁,久则凝淀如石,浣衣发面,亦去垢发面”.此处“石碱条”是指( )
0 157917 157925 157931 157935 157941 157943 157947 157953 157955 157961 157967 157971 157973 157977 157983 157985 157991 157995 157997 158001 158003 158007 158009 158011 158012 158013 158015 158016 158017 158019 158021 158025 158027 158031 158033 158037 158043 158045 158051 158055 158057 158061 158067 158073 158075 158081 158085 158087 158093 158097 158103 158111 203614
| A. | K2CO3 | B. | Na2SO4 | C. | Ca(OH)2 | D. | Na2CO3 |
 短周期主族元素A、B、C、D、E,原子序数依次增大,A元素的单质常温常温下是最轻的气体,B元素所形成化合物种类最多,C的最高价氧化物对应水化物民其气态氢化物乙能够化合形成盐丙;D元素的离子半径是同周期元素形成的简单离子中最小的.
短周期主族元素A、B、C、D、E,原子序数依次增大,A元素的单质常温常温下是最轻的气体,B元素所形成化合物种类最多,C的最高价氧化物对应水化物民其气态氢化物乙能够化合形成盐丙;D元素的离子半径是同周期元素形成的简单离子中最小的.