7.下列离子方程式书写正确的是( )
| A. | 氯气溶于水:Cl2+H2O═2H++Cl-+ClO- | |
| B. | 硫酸铝溶液中加入足量氨水:Al3++4OH-═AlO${\;}_{2}^{-}$+2H2O | |
| C. | FeSO4溶液与稀硝酸反应:3Fe2++NO${\;}_{3}^{-}$+4H+═3Fe3++NO↑+2H2O | |
| D. | 碳酸氢铵和足量氢氧化钠溶液反应:NH${\;}_{4}^{+}$+OH-═NH3•H2O |
5.如表是50mL稀盐酸和1g碳酸钙反应的实验数据:
分析上述数据,回答下列问题:
(1)本反应属于放热反应(填吸热或放热),实验中的所有反应,反应前后溶液的温度变化值相近(约为20℃),推测其原因是反应掉碳酸钙的量相同,放出的热量相同.
(2)实验6和7表明,温度对反应速率有影响,温度越高反应速率
越快,能表明同一规律的实验还有8和9(填实验序号).
(3)根据实验1、3、4、6、8可以得出条件对反应速率的影响规律是其它条件一定,反应物浓度越大,反应速率越快.
(4)本实验中影响反应速率的其它因素还有反应物的接触面积,能表明这一规律的实验序号是1、2与4和5.
| 实验 序号 | 碳酸钙 状态 | c(HCl) /mol•L-1 | 溶液温度/℃ | 碳酸钙消失 时间/s | |
| 反应前 | 反应后 | ||||
| 1 | 粒状 | 0.5 | 20 | 39 | 400 |
| 2 | 粉末 | 0.5 | 20 | 40 | 60 |
| 3 | 粒状 | 0.6 | 20 | 41 | 280 |
| 4 | 粒状 | 0.8 | 20 | 40 | 200 |
| 5 | 粉末 | 0.8 | 20 | 40 | 30 |
| 6 | 粒状 | 1.0 | 20 | 40 | 120 |
| 7 | 粒状 | 1.0 | 30 | 50 | 40 |
| 8 | 粒状 | 1.2 | 20 | 40 | 90 |
| 9 | 粒状 | 1.2 | 25 | 45 | 40 |
(1)本反应属于放热反应(填吸热或放热),实验中的所有反应,反应前后溶液的温度变化值相近(约为20℃),推测其原因是反应掉碳酸钙的量相同,放出的热量相同.
(2)实验6和7表明,温度对反应速率有影响,温度越高反应速率
越快,能表明同一规律的实验还有8和9(填实验序号).
(3)根据实验1、3、4、6、8可以得出条件对反应速率的影响规律是其它条件一定,反应物浓度越大,反应速率越快.
(4)本实验中影响反应速率的其它因素还有反应物的接触面积,能表明这一规律的实验序号是1、2与4和5.
4. 某实验小组以H2O2分解为例,研究浓度、催化剂、溶液的酸碱性①对反应速率的影响.在常温下按照如表方案完成实验.
某实验小组以H2O2分解为例,研究浓度、催化剂、溶液的酸碱性①对反应速率的影响.在常温下按照如表方案完成实验.
(1)催化剂能加快化学反应速率的原因是降低了反应的活化能.
(2)实验①和②的目的是探究浓度对反应速率的影响.
实验时由于没有观察到明显现象而无法得出结论.资料显示,通常条件下H2O2稳定,不易分解.为了达到实验目的,你对原实验方案的改进是向反应物中加入等量同种催化剂(或将盛有反应物的试管放入同一热水浴中).
(3)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如图所示.分析图示能够得出的实验结论是碱性环境能增大H2O2分解的速率,酸性环境能减小H2O2分解的速率.
 某实验小组以H2O2分解为例,研究浓度、催化剂、溶液的酸碱性①对反应速率的影响.在常温下按照如表方案完成实验.
某实验小组以H2O2分解为例,研究浓度、催化剂、溶液的酸碱性①对反应速率的影响.在常温下按照如表方案完成实验.| 编号 | 反应物 | 催化剂 |
| ① | 10mL 2%H2O2溶液 | 无 |
| ② | 10mL 5% H2O2溶液 | 无 |
| ③ | 10mL 5%H2O2溶液 | 1mL 0.1mol•L-1FeCl3溶液 |
| ④ | 10mL 5% 5H2O2溶液+少量HCl溶液 | 1mL 0.1mol•L-1FeCl3溶液 |
| ⑤ | 10mL 5%H2O2溶液+少量NaOH溶液 | 1mL 0.1mol•L-1FeCl3溶液 |
(2)实验①和②的目的是探究浓度对反应速率的影响.
实验时由于没有观察到明显现象而无法得出结论.资料显示,通常条件下H2O2稳定,不易分解.为了达到实验目的,你对原实验方案的改进是向反应物中加入等量同种催化剂(或将盛有反应物的试管放入同一热水浴中).
(3)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如图所示.分析图示能够得出的实验结论是碱性环境能增大H2O2分解的速率,酸性环境能减小H2O2分解的速率.
3.(1)下表中有三组物质,每组均有甲、乙、丙三种物质(酸、碱、盐均为溶液).
根据该表回答问题:
第Ⅲ组中有一种物质与第Ⅰ组中的所有物质反应,这种物质是H2SO4.
第Ⅱ组物质中,跟第Ⅰ组所有物质都不能发生反应的是NaOH.
(2)双氧水H2O2可作为矿业废液消毒剂,可以消除采矿业废液中的氰化物(如KCN)化学方程式为:KCN+H2O2+H2O═KHCO3+A↑(已配平)①生成物A的化学式为NH3;②反应中被氧化的元素为C;③该反应中的氧化剂是H2O2.
(3)写出下列物质在水溶液里的电离方程式:硫酸铁Fe2(SO4)3=2Fe3++3SO42-,氯酸钾KClO3=K++ClO3-,NaHSO4在熔融状态下的电离方程式是NaHSO4=Na++HSO4-.
(4)下列说法中正确的是BD.
A.NaHSO4属于酸 B.NaHSO4属于酸式盐
C.NaHSO4溶液属于电解质 D.NaHSO4溶液能与Zn反应生成氢气
(5)Fe(OH)3胶体的制备方法在沸腾的蒸馏水中加入饱和氯化铁溶液,当溶液变为红褐色时立即停止加热.
| 第Ⅰ组 | 第Ⅱ组 | 第Ⅲ组 | |
| 甲 | BaCl2 | HCl | Cu(NO3)2 |
| 乙 | Fe2O3 | K2SO4 | H2SO4 |
| 丙 | Fe | NaOH | MgCl2 |
第Ⅲ组中有一种物质与第Ⅰ组中的所有物质反应,这种物质是H2SO4.
第Ⅱ组物质中,跟第Ⅰ组所有物质都不能发生反应的是NaOH.
(2)双氧水H2O2可作为矿业废液消毒剂,可以消除采矿业废液中的氰化物(如KCN)化学方程式为:KCN+H2O2+H2O═KHCO3+A↑(已配平)①生成物A的化学式为NH3;②反应中被氧化的元素为C;③该反应中的氧化剂是H2O2.
(3)写出下列物质在水溶液里的电离方程式:硫酸铁Fe2(SO4)3=2Fe3++3SO42-,氯酸钾KClO3=K++ClO3-,NaHSO4在熔融状态下的电离方程式是NaHSO4=Na++HSO4-.
(4)下列说法中正确的是BD.
A.NaHSO4属于酸 B.NaHSO4属于酸式盐
C.NaHSO4溶液属于电解质 D.NaHSO4溶液能与Zn反应生成氢气
(5)Fe(OH)3胶体的制备方法在沸腾的蒸馏水中加入饱和氯化铁溶液,当溶液变为红褐色时立即停止加热.
19.下面是X和Y反应的微观过程示意图,下列有关说法中不正确的是( )

| A. | 该过程中有极性键的断裂和形成 | B. | 该过程中的X和Y均为活化分子 | ||
| C. | 加入催化剂能增大X和Y分子的能量 | D. | 该过程不能消除大气污染物 |
18.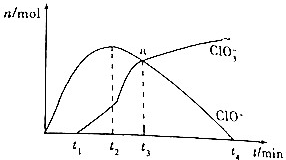 工业上把Cl2通入冷NaOH溶液中制得漂白液(主要成分为NaClO),某化学小组在一定温度下将氯气缓缓通入NaOH溶液,模拟实验得到ClO-、ClO${\;}_{3}^{-}$的物质的量(mol)与反应时间t(min)的关系如图所示.下列说法错误的是( )
工业上把Cl2通入冷NaOH溶液中制得漂白液(主要成分为NaClO),某化学小组在一定温度下将氯气缓缓通入NaOH溶液,模拟实验得到ClO-、ClO${\;}_{3}^{-}$的物质的量(mol)与反应时间t(min)的关系如图所示.下列说法错误的是( )
 工业上把Cl2通入冷NaOH溶液中制得漂白液(主要成分为NaClO),某化学小组在一定温度下将氯气缓缓通入NaOH溶液,模拟实验得到ClO-、ClO${\;}_{3}^{-}$的物质的量(mol)与反应时间t(min)的关系如图所示.下列说法错误的是( )
工业上把Cl2通入冷NaOH溶液中制得漂白液(主要成分为NaClO),某化学小组在一定温度下将氯气缓缓通入NaOH溶液,模拟实验得到ClO-、ClO${\;}_{3}^{-}$的物质的量(mol)与反应时间t(min)的关系如图所示.下列说法错误的是( )| A. | 参加反应所需要NaOH与氯气的物质的量之比一定为2:1 | |
| B. | a点时溶液中n(NaCl):n(NaClO3):n(NaClO)=6:1:1 | |
| C. | t2~t4min,ClO-的物质的量下降的原因可能是3ClO-═2Cl-+ClO${\;}_{3}^{-}$ | |
| D. | 使用漂白液时,为了增强漂白效果,可以向漂白液中加入浓盐酸 |
17. 下列关于物质的分离提纯不正确的是( )
下列关于物质的分离提纯不正确的是( )
0 157861 157869 157875 157879 157885 157887 157891 157897 157899 157905 157911 157915 157917 157921 157927 157929 157935 157939 157941 157945 157947 157951 157953 157955 157956 157957 157959 157960 157961 157963 157965 157969 157971 157975 157977 157981 157987 157989 157995 157999 158001 158005 158011 158017 158019 158025 158029 158031 158037 158041 158047 158055 203614
 下列关于物质的分离提纯不正确的是( )
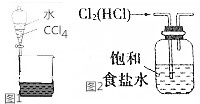
下列关于物质的分离提纯不正确的是( )| A. | 用如图1所示装置分离CCl4和水 | |
| B. | 除去苯中的少量苯酚,加入适量浓溴水,过滤 | |
| C. | 实验室用如图2所示装置除去Cl2中的少量HCl | |
| D. | 除去O2中混有得得少量SO2,可将混合气体依次通过盛有酸性KMnO4溶液、浓硫酸的洗气瓶 |
 ;
;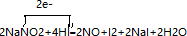 .
.