19. 把在空气中久置的铝片5.0g投入盛有50mL 0.1mol•L-1盐酸溶液的烧杯中,该铝片与盐酸反应,产生氢气的速率v(H2)与反应时间t的关系,可用如图所示的坐标曲线来表示,下列推论错误的是( )
把在空气中久置的铝片5.0g投入盛有50mL 0.1mol•L-1盐酸溶液的烧杯中,该铝片与盐酸反应,产生氢气的速率v(H2)与反应时间t的关系,可用如图所示的坐标曲线来表示,下列推论错误的是( )
 把在空气中久置的铝片5.0g投入盛有50mL 0.1mol•L-1盐酸溶液的烧杯中,该铝片与盐酸反应,产生氢气的速率v(H2)与反应时间t的关系,可用如图所示的坐标曲线来表示,下列推论错误的是( )
把在空气中久置的铝片5.0g投入盛有50mL 0.1mol•L-1盐酸溶液的烧杯中,该铝片与盐酸反应,产生氢气的速率v(H2)与反应时间t的关系,可用如图所示的坐标曲线来表示,下列推论错误的是( )| A. | O→a段不产生氢气是因为表面的氧化物隔离了铝和稀盐酸 | |
| B. | b→c段产生氢气的速率增加较快的主要原因之一是温度升高 | |
| C. | t=c时刻,反应处于平衡 | |
| D. | t>c时,产生氢气的速率降低的主要原因是溶液中H+浓度下降 |
18.100mL 2mol/L 稀硫酸与1g锌粒反应,在一定温度下为了减缓反应的速率,而又不影响生成氢气的总量,可向反应物中加入( )
| A. | 硫酸钠固体 | B. | 硫酸铜固体 | C. | 氯化钠溶液 | D. | 硝酸钾溶液 |
15.下列各组物质的熔点均与所含化学键的键能有关的是( )
| A. | CaO与CO2 | B. | SiC与SiO2 | C. | NaCl与HCl | D. | Cl2与I2 |
13.高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压,高铁电池的总反为:3Zn+2K2FeO4+8H2O$?_{充电}^{放电}$3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是( )
0 157827 157835 157841 157845 157851 157853 157857 157863 157865 157871 157877 157881 157883 157887 157893 157895 157901 157905 157907 157911 157913 157917 157919 157921 157922 157923 157925 157926 157927 157929 157931 157935 157937 157941 157943 157947 157953 157955 157961 157965 157967 157971 157977 157983 157985 157991 157995 157997 158003 158007 158013 158021 203614
| A. | 放电时负极反应式为:Zn-2e-+2OH-=Zn(OH)2 | |
| B. | 放电时每转移3mol电子,正极有1 mol K2FeO4被还原 | |
| C. | 充电时阴极附近溶液的碱性增强 | |
| D. | 放电时正极反应式为:Fe(OH)3-3e-+5OH-=FeO42-+4H2O |
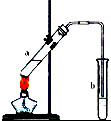 ①生成液体W的化学方程式为CH3CH2OH+CH3COOH$?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O;
①生成液体W的化学方程式为CH3CH2OH+CH3COOH$?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O;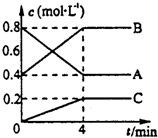 一定条件下,A、B、C三种气体在绝热密闭容器中随反应进行,温度升高;且各物质浓度的变化情况如图所示,通过分析回答:
一定条件下,A、B、C三种气体在绝热密闭容器中随反应进行,温度升高;且各物质浓度的变化情况如图所示,通过分析回答: