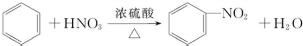
10.用括号内的试剂和分离方法,除去下列物质中的少量杂质,正确的是( )
| A. | 乙醇中的水(生石灰,蒸馏) | B. | 乙烷中的乙烯(酸性KMnO4溶液,洗气) | ||
| C. | 溴苯中的溴(KI溶液,分液) | D. | 乙酸乙酯中的乙酸(NaOH溶液,蒸馏) |
9.设NA为阿伏加德罗常数值.下列有关叙述不正确的是( )
| A. | 标准状况下,2.24 L CCl4含有的共价键数为0.4NA | |
| B. | 0.2 mol C2H6分子中一定存在0.2NA个碳碳单键 | |
| C. | 1 mol Fe溶于过量硝酸,电子转移数为3NA | |
| D. | 14 g乙烯和丙烯混合气体中的氢原子数为2NA |
8.化学与生活密切相关,下列有关说法错误的是( )
| A. | 用灼烧的方法可以区分蚕丝和人造纤维 | |
| B. | 医用消毒酒精中乙醇的浓度为95% | |
| C. | 加热能杀死流感病毒是因为蛋白质受热变性 | |
| D. | 食用油反复加热会产生稠环芳香烃等有害物质 |
7.某小组利用H2C2O4溶液和酸性KMnO4溶液反应来探究“条件对化学反应速率的影响”.
(1)已知:KMnO4+H2C2O4+H2SO4→MnSO4+K2SO4+CO2↑+H20(未配平),向酸性KMnO4溶液中加入一定量的H2C2O4溶液,当溶液中的KMnO4耗尽后,紫色溶液将褪去.为确保能观察到紫色褪去,H2C2O4与KMnO4初始的物质的量需要满足的关系为n(H2C2O4):n(KMnO4)≥2.5.
(2)为探究反应物浓度对化学反应速率的影响,该小组设计了如下实验方案
表中x=2.0ml,理由是保证其它条件不变,只改变反应物H2C2O4浓度,从而达到对照实验的目的.
(1)已知:KMnO4+H2C2O4+H2SO4→MnSO4+K2SO4+CO2↑+H20(未配平),向酸性KMnO4溶液中加入一定量的H2C2O4溶液,当溶液中的KMnO4耗尽后,紫色溶液将褪去.为确保能观察到紫色褪去,H2C2O4与KMnO4初始的物质的量需要满足的关系为n(H2C2O4):n(KMnO4)≥2.5.
(2)为探究反应物浓度对化学反应速率的影响,该小组设计了如下实验方案
| 实验序号 | 反应温度/℃ | H2C2O4溶液 | 酸性KMnO4溶液 | H2O | ||
| V/mL | c(mol•L-1) | V/mL | c(mol•L-1) | V/mL | ||
| ① | 25 | 8.0 | 0.20 | 5.0 | 0.010 | 0 |
| ② | 25 | 6.0 | 0.20 | 5.0 | 0.010 | x |
3.活性炭可处理大气污染物NO.T℃时,在1L密闭容器中加入NO气体和炭粉,发生反应生成两种气体A和B,测得各物质的物质的量如下:
(1)2min内,用NO表示该反应的平均速率v(NO)=0.03mol•L-1•min-1.
(2)该反应的化学方程式是C+2NO?N2+CO2.
(3)一定条件下,在密闭恒容的容器中,能表示上述反应达到化学平衡状态的是②④.
①v(NO):v(A):v(B)=2:1:1
②混合气体的密度不再改变
③总压强不再改变
④混合气体的平均相对分子质量不再改变
 (4)碳元素可形成数量众多,分布极广的有机化合物,其中甲醇是常见的燃料,甲醇燃料电池的结构示意图如下,一极通入甲醇,另外一极通入氧气;电解质溶液是稀硫酸,电池工作时总反应式:2CH3OH+3O2=2CO2+4H2O.
(4)碳元素可形成数量众多,分布极广的有机化合物,其中甲醇是常见的燃料,甲醇燃料电池的结构示意图如下,一极通入甲醇,另外一极通入氧气;电解质溶液是稀硫酸,电池工作时总反应式:2CH3OH+3O2=2CO2+4H2O.
①a处通入的物质是CH3OH,电极反应式为:CH3OH-6e-+H2O=CO2+6H+;
②b处电极反应式为3O2+12e-+12H+=6H2O;
③电池工作时H+由负极移向正极(填正、负极).
0 157813 157821 157827 157831 157837 157839 157843 157849 157851 157857 157863 157867 157869 157873 157879 157881 157887 157891 157893 157897 157899 157903 157905 157907 157908 157909 157911 157912 157913 157915 157917 157921 157923 157927 157929 157933 157939 157941 157947 157951 157953 157957 157963 157969 157971 157977 157981 157983 157989 157993 157999 158007 203614
| 活性炭/mol | NO/mol | A/mol | B/mol | |
| 起始状态 | 2.030 | 0.100 | 0 | 0 |
| 2min时 | 2.000 | 0.040 | 0.030 | 0.030 |
(2)该反应的化学方程式是C+2NO?N2+CO2.
(3)一定条件下,在密闭恒容的容器中,能表示上述反应达到化学平衡状态的是②④.
①v(NO):v(A):v(B)=2:1:1
②混合气体的密度不再改变
③总压强不再改变
④混合气体的平均相对分子质量不再改变
 (4)碳元素可形成数量众多,分布极广的有机化合物,其中甲醇是常见的燃料,甲醇燃料电池的结构示意图如下,一极通入甲醇,另外一极通入氧气;电解质溶液是稀硫酸,电池工作时总反应式:2CH3OH+3O2=2CO2+4H2O.
(4)碳元素可形成数量众多,分布极广的有机化合物,其中甲醇是常见的燃料,甲醇燃料电池的结构示意图如下,一极通入甲醇,另外一极通入氧气;电解质溶液是稀硫酸,电池工作时总反应式:2CH3OH+3O2=2CO2+4H2O.①a处通入的物质是CH3OH,电极反应式为:CH3OH-6e-+H2O=CO2+6H+;
②b处电极反应式为3O2+12e-+12H+=6H2O;
③电池工作时H+由负极移向正极(填正、负极).
 下列给出了烃及烃的衍生物A、B、C、D、E的相关信息:
下列给出了烃及烃的衍生物A、B、C、D、E的相关信息: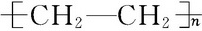 .
.