12.设NA为阿伏加德罗常数,下列说法错误的是( )
| A. | 1 mol H2O所含电子数为10NA | |
| B. | 1 mol Al与足量的稀盐酸溶液反应生成氢气1.5 mol | |
| C. | 在标准状况下,0.5NA Cl2所占的体积约是11.2 L | |
| D. | 在非标准状况下,22.4 L O2含有的分子数一定不是NA |
10.下列实验装置、试剂选用或操作正确的是( )
| A. |  干燥Cl2 | B. |  稀释浓硫酸 | C. |  制取蒸馏 | D. |  称量NaOH |
9.某合作学习小组讨论辨析以下说法正确的是( )
①粗盐和酸雨都是混合物
②硅是光导纤维的主要成分
③冰和干冰既是纯净物又是化合物
④不锈钢和目前流通的硬币都是合金
⑤盐酸和食醋既是化合物又是酸
⑥纯碱和熟石灰都是碱
⑦豆浆、雾、烟都是胶体
⑧利用丁达尔效应可以区分溶液和胶体.
①粗盐和酸雨都是混合物
②硅是光导纤维的主要成分
③冰和干冰既是纯净物又是化合物
④不锈钢和目前流通的硬币都是合金
⑤盐酸和食醋既是化合物又是酸
⑥纯碱和熟石灰都是碱
⑦豆浆、雾、烟都是胶体
⑧利用丁达尔效应可以区分溶液和胶体.
| A. | ③④⑤⑥⑦ | B. | ①②③④⑥ | C. | ①③④⑦⑧ | D. | ①②④⑤⑧ |
8.下列实验“操作和现象”与“结论”对应关系正确的是( )


| A. | a图,滴加乙醇,试管中橙色溶液变为绿色,乙醇发生取代反应生成乙酸 | |
| B. | b图,右边试管中产生气泡较为迅速,说明氯化铁的催化效果比二氧化锰好 | |
| C. | c图,根据试管中收集到无色气体,不能验证铜与稀硝酸的反应产物是NO | |
| D. | d图,试管中先有白色沉淀、后有黑色沉淀生成,能确定Ksp(AgCl)>Ksp(Ag2S) |
6.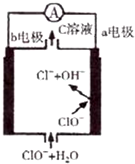 镁一次氯酸盐电池的工作原理如图,该电池反应为:Mg+ClO-+H2O═Mg(OH)2+Cl-.下列有关说法正确的是( )
镁一次氯酸盐电池的工作原理如图,该电池反应为:Mg+ClO-+H2O═Mg(OH)2+Cl-.下列有关说法正确的是( )
 镁一次氯酸盐电池的工作原理如图,该电池反应为:Mg+ClO-+H2O═Mg(OH)2+Cl-.下列有关说法正确的是( )
镁一次氯酸盐电池的工作原理如图,该电池反应为:Mg+ClO-+H2O═Mg(OH)2+Cl-.下列有关说法正确的是( )| A. | 电池工作时,正极a附近的pH将不断增大 | |
| B. | 电池工作时,C溶液中的溶质是MgCl2 | |
| C. | 负极反应式:ClO-+2e-+H2O=Cl-+2OH- | |
| D. | b电极发生还原反应,每转移0.1 mol电子,理论上生成0.1 mol Cl- |
5.下列有关实验原理或实验操作正确的是( )


| A. | 用pH试纸测量新制氯水的pH | |
| B. | 用量筒量取 20mL 0.5000mol•L-1 H2SO4溶液于烧杯中,加水80mL,配制成0.1000mol•L-1H2SO4溶液 | |
| C. | 图1所示装置可用于吸收NH3或HC1气体,并防止倒吸 | |
| D. | 实验室用图2所示装置除去Cl2中的少量HC1 |
4.X、Y、Z、W、R是原子序数依次增大的短周期主族元素,X是原子半径最小的元素,Y的最高正价与最低负价的代数和为0,Z的二价阳离子与氖原子具行相同的核外电子排布,W原子最外层电子数是最内层电子数的3倍.下列说法正确的是( )
| A. | X与Y形成的化合物只有一种 | |
| B. | 原子半径:r(Z)<r(R) | |
| C. | R的氯化物的热稳定性比W的强 | |
| D. | Y的最高价氧化物对应水化物的酸性比W的强 |
3.某反应2A(g)+B(g)?C(g)经10s后A的物质的量浓度为0.2mol/L,B的物质的浓度降低了0.02mol/L,
则A物质的起始浓度为( )
0 157807 157815 157821 157825 157831 157833 157837 157843 157845 157851 157857 157861 157863 157867 157873 157875 157881 157885 157887 157891 157893 157897 157899 157901 157902 157903 157905 157906 157907 157909 157911 157915 157917 157921 157923 157927 157933 157935 157941 157945 157947 157951 157957 157963 157965 157971 157975 157977 157983 157987 157993 158001 203614
则A物质的起始浓度为( )
| A. | 0.24 mol/L | B. | 0.6 mol/L | C. | 2.4 mol/L | D. | 4.2 mol/L |
 与NaOH的醇溶液共热制备CH3-CH=CH2.
与NaOH的醇溶液共热制备CH3-CH=CH2.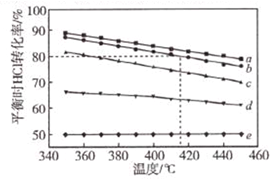 文献报道:利用氯化氢氧化反应一脱水耦合工艺,可用有机氯化工艺的副产品氯化氢为原料制备氯气,实现氯的循环利用,原理为4HCl(g)+O2(g)?2Cl2(g)+2H2O(g).将HC1和O2分别以5种物质的量比:①1:1 ②2:1 ③4:1 ④6:1 ⑤8:1,向五个容积可变的容器中投料时,反应温度对HCl平衡转化氯影响的曲线如图.
文献报道:利用氯化氢氧化反应一脱水耦合工艺,可用有机氯化工艺的副产品氯化氢为原料制备氯气,实现氯的循环利用,原理为4HCl(g)+O2(g)?2Cl2(g)+2H2O(g).将HC1和O2分别以5种物质的量比:①1:1 ②2:1 ③4:1 ④6:1 ⑤8:1,向五个容积可变的容器中投料时,反应温度对HCl平衡转化氯影响的曲线如图.