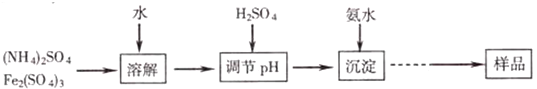
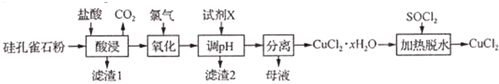
6.冰铜矿的主要成分是Cu2S、FeS,含有少许Al2O3和SiO2杂质.由冰铜矿冶炼金属铜的流程如下:

已知各离子沉淀的范围如下表
请回答下列问题:
(1)将冰铜矿粉碎的目的是提高浸出率,另外一种提高浸出率的措施是升高温度或者增大浸取剂浓度等.
(2)溶液1的成分是NaAlO2、Na2SiO3、NaOH,若向其中通入足量的CO2可以析出的沉淀是H2SiO3、Al(OH)3,
此时溶液中的溶质将变成NaHCO3.
(3)沉淀1加入H2O2和稀H2SO4后,溶液中阴离子只有SO42-,金属阳离子有Cu2+ 和F3+,则该过程的离子方程式为:2H++Cu2S+5H2O2═2Cu2++SO42-+6H2O,2H++2FeS+9H2O2═2Fe3++2SO42-+10H2O.
(4)溶液2调节的pH范围为3.4≤pH<6.7.
(5>对红褐色沉淀进行洗涤并干燥处理,可以得到纯净的Fe(OH)3,可用于制备红色颜料Fe2O3.检验红褐色沉淀是否洗净的方法是取最后一次洗涤液于试管中,滴加BaCl2溶液,若不产生白色沉淀,则沉淀已经洗净.
(6)用惰性电极对溶液3进行电解,电解CuSO4溶液的化学方程式为:2CuSO4+2H2O $\frac{\underline{\;通电\;}}{\;}$2Cu+O2↑+2H2SO4;
当两极共产生标准状况下44.8L气体且阴阳两极产生的气体体积之比为1:1时,则析出的铜的质量为64g.

已知各离子沉淀的范围如下表
| 离子 | Fe3+ | Fe2+ | Cu2+ |
| 开始沉淀pH | 1,9 | 7.0 | 6,7 |
| 沉淀完全pH | $\frac{3}{4}$ | 9.0 | 10.0 |
(1)将冰铜矿粉碎的目的是提高浸出率,另外一种提高浸出率的措施是升高温度或者增大浸取剂浓度等.
(2)溶液1的成分是NaAlO2、Na2SiO3、NaOH,若向其中通入足量的CO2可以析出的沉淀是H2SiO3、Al(OH)3,
此时溶液中的溶质将变成NaHCO3.
(3)沉淀1加入H2O2和稀H2SO4后,溶液中阴离子只有SO42-,金属阳离子有Cu2+ 和F3+,则该过程的离子方程式为:2H++Cu2S+5H2O2═2Cu2++SO42-+6H2O,2H++2FeS+9H2O2═2Fe3++2SO42-+10H2O.
(4)溶液2调节的pH范围为3.4≤pH<6.7.
(5>对红褐色沉淀进行洗涤并干燥处理,可以得到纯净的Fe(OH)3,可用于制备红色颜料Fe2O3.检验红褐色沉淀是否洗净的方法是取最后一次洗涤液于试管中,滴加BaCl2溶液,若不产生白色沉淀,则沉淀已经洗净.
(6)用惰性电极对溶液3进行电解,电解CuSO4溶液的化学方程式为:2CuSO4+2H2O $\frac{\underline{\;通电\;}}{\;}$2Cu+O2↑+2H2SO4;
当两极共产生标准状况下44.8L气体且阴阳两极产生的气体体积之比为1:1时,则析出的铜的质量为64g.
1.25℃时,下列溶液中微粒的物质的量浓度关系正确的是( )
| A. | 0.lmol•L-lNaHC2O4溶液(pH=5.5):c(Na+)>c( HC2O4-)>c(H2C2O4)>c(C2O42- ) | |
| B. | 0.lmol•L-1NaHS 溶液:C(OH-)+c(S2-)=c( H+)+c(H2S) | |
| C. | 0.lmol•L-1CH3COOH 溶液和 0.lmol•L-1CH3COONa 溶液等体积混合:c(Na+)>c(CH3COOH)>c(CH3COO-)>c(H+)>c( OH-) | |
| D. | 0.lmol•L-lNH4HSO4 溶液中滴加 0.lmol•L-1NaOH 溶液至中性:c(Na+ )>c(SO42- )>c(NH4+ )>c(OH-)=c(H+) |
20.下列物质转化在给定条件下能实现的是( )
| A. | FeS2$\stackrel{煅烧}{→}$SO3$\stackrel{H_{2}O}{→}$H2SO4 | |
| B. | NaCl(aq)$\stackrel{电解}{→}$Na$\stackrel{O_{2}}{→}$Na2O2 | |
| C. | Fe$\stackrel{稀H_{2}SO_{4}}{→}$FeSO4(aq)$\stackrel{NaOH(aq)}{→}$Fe(OH)2$\stackrel{空气中灼烧}{→}$Fe2O3 | |
| D. | Fe2O3$\stackrel{盐酸}{→}$FeCl3(aq)$\stackrel{Cu}{→}$Fe |
19.下列离子方程式正确的是( )
| A. | 金属钠与水反应:Na+2H2O═Na++2OH-+H2↑ | |
| B. | Cu与浓硝酸反应制 NO2:Cu+4HNO3(浓)═Cu2++2 NO3-+NO2↑+2H2O | |
| C. | 向同浓度的NaOH和Na2CO3,的混合液中加少量稀盐酸:CO32-+2H+═CO2↑+3H2O | |
| D. | 将 NaHSO4与 Ba(OH)2溶液混合至中性:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O |
18.下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 0.1mol•L -1AgNO3,溶液:H+、K+、SO42-、I- | |
| B. | c( H+ )/c( OH-)=1012的溶液中:NH4+、Al3+、NO3-、Cl- | |
| C. | 由水电离的 c(H+)=1×10-14mol•L-1的溶液中:Ca2+、K+、Cl-、HCO3- | |
| D. | 甲基橙呈红色的溶液中:Na+、CO32-、Fe3+、Cl- |
17.下列有关化学用语表示正确的是( )
0 157795 157803 157809 157813 157819 157821 157825 157831 157833 157839 157845 157849 157851 157855 157861 157863 157869 157873 157875 157879 157881 157885 157887 157889 157890 157891 157893 157894 157895 157897 157899 157903 157905 157909 157911 157915 157921 157923 157929 157933 157935 157939 157945 157951 157953 157959 157963 157965 157971 157975 157981 157989 203614
| A. | NH4Br的电子式: | |
| B. | 葡萄糖的结构简式:C6H12O6 | |
| C. | 水分子的比例模型: | |
| D. | 原子核内有18个中子的氣原子:1735Cl |
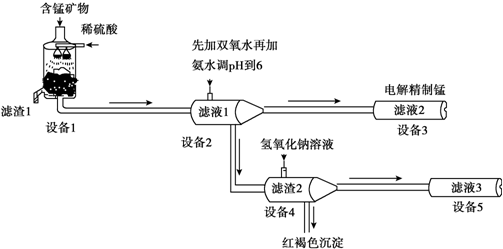
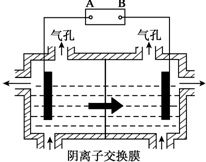 (5)设备3中用阴离子膜法提取金属锰的电解装置如图:
(5)设备3中用阴离子膜法提取金属锰的电解装置如图: