5.A、B为短周期元素,二者可以组合成多种中学生所熟知的化合物.在这些化合物中,A与B的原子个数比为A:B=1:2.已知A的原子序数为n,B的原子序数是①n+2 ②n+3 ③n+4 ④n+5 ⑤n+8 ⑥n-5 ⑦n-7 ⑧n-8中的几种,其中不符合题目要求的是( )
| A. | ①④ | B. | ②⑧ | C. | ③⑤ | D. | ⑥⑦ |
1.下列说法正确的是( )
| A. | 漂白粉的有效成份是氯酸钙 | B. | 氟化氢溶于水形成的氢氟酸是强酸 | ||
| C. | 碘化钾水溶液能使淀粉变蓝 | D. | 氟气通入水中有氧气生成 |
20.某同学根据H2S和浓H2SO4的性质做出下列推测,其中正确的是( )
| A. | 浓H2SO4具有强氧化性是因为其中含+6价S,所有只要含最高价+6价S的化合物就具有强氧化性 | |
| B. | H2S中的S处于最低价,因此其不可能具有氧化性 | |
| C. | 浓H2SO4可把Na2SO3氧化 | |
| D. | 因为元素化合价变化以相邻价态之间转化最容易,因此发生氧化还原反应时,浓H2SO4对应的产物一般为SO2 |
19.下列物质的电子式书写正确的是( )
| A. | MgCl2  | B. | CCl4  | C. | CO2  | D. | Na2O  |
18.某小组为研究电化学原理,设计如图装置.下列叙述不正确的是( )


| A. | a和b用导线连接时,该装置为原电池,铁片为负极,发生氧化反应 | |
| B. | a和b用导线连接时,Pt片上发生的反应为:Cu2++2e-═Cu | |
| C. | a和b分别连接直流电源正、负极时,该装置为电解池,Pt片为阳极,电极反应式为:4OH--4e-═O2↑+2H2O | |
| D. | a和b分别连接直流电源正、负极时,Cu2+向Pt电极移动 |
17.不能实现下列物质间直接转换的是( )
0 157791 157799 157805 157809 157815 157817 157821 157827 157829 157835 157841 157845 157847 157851 157857 157859 157865 157869 157871 157875 157877 157881 157883 157885 157886 157887 157889 157890 157891 157893 157895 157899 157901 157905 157907 157911 157917 157919 157925 157929 157931 157935 157941 157947 157949 157955 157959 157961 157967 157971 157977 157985 203614

| A. | 铝 | B. | 碳 | C. | 硫 | D. | 氮 |
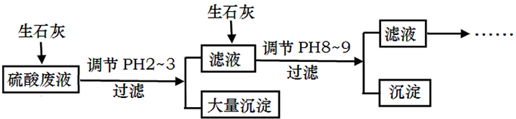
 工业尾气SO2有多种吸收和处理方法.
工业尾气SO2有多种吸收和处理方法.