6.设NA表示阿伏加德罗常数,下列叙述中,正确的是( )
| A. | 25℃、101kPa时,11.2L H2中含有的原子数为NA | |
| B. | 78g Na2O2与足量水充分反应时电子转移数为2NA | |
| C. | 等质量的CO与CO2中所含碳原子数之比为11:7 | |
| D. | 将98g H2SO4溶解于500mL水中,所得溶液中硫酸的物质的量浓度为2 mol/L |
3.按要求回答下列问题
(1)写出下列物质在水中的电离方程式
①NaHCO3NaHCO3═Na++HCO3-;②HClOHClO?H++ClO-.
(2)若要除去下列溶液中的杂质(括号内为杂质),请将选用的试剂及有关反应的离子方程式填入下表的空白处:
(3)镁着火不能用二氧化碳来灭火,理由是2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C(用化学方程式表示)
(4)写出离子方程式CO32-+2H+═CO2↑+H2O所对应的化学方程式Na2CO3+2HCl=2NaCl+CO2+H2O.
(1)写出下列物质在水中的电离方程式
①NaHCO3NaHCO3═Na++HCO3-;②HClOHClO?H++ClO-.
(2)若要除去下列溶液中的杂质(括号内为杂质),请将选用的试剂及有关反应的离子方程式填入下表的空白处:
| 物质(杂质) | 试剂 | 有关离子方程式 |
| NaHCO3(Na2CO3) | ||
| FeCl2(FeCl3) |
(4)写出离子方程式CO32-+2H+═CO2↑+H2O所对应的化学方程式Na2CO3+2HCl=2NaCl+CO2+H2O.
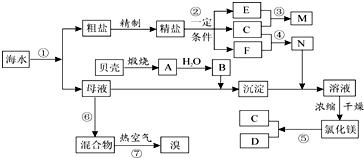
20.重铬酸钠(Na2Cr2O7•2H2O)俗称红矾钠,在工业方面有广泛用途.我国目前主要是以铬铁矿(主要成份为FeO•Cr2O3,还含有Al2O3、MgO、SiO2等杂质)为主要原料进行生产,其主要工艺流程如图:

①中涉及的主要反应有:
主反应:4FeO•Cr2O3+8Na2CO3+7O2$\frac{\underline{\;\;△\;\;}}{\;}$8Na2CrO4+2Fe2O3+8CO2
副反应:SiO2+Na2CO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2SiO3+CO2↑、Al2O3+Na2CO3$\frac{\underline{\;\;△\;\;}}{\;}$2NaAlO2+CO2↑
部分阳离子以氢氧化物形式完全沉淀时溶液的pH:
试回答下列问题:
(1)“①”中反应是在回转窑中进行,反应时需不断搅拌,其作用是使反应物接触更充分,加快反应速率.
(2)“③”中调节pH至4.7,目的是除去溶液中的AlO2-、SiO32-.
(3)“⑤”中加硫酸酸化的目的是使CrO42-转化为Cr2O72-,请写出该平衡转化的离子方程式:2CrO42-+2H+?Cr2O72-+H2O.
(4)称取重铬酸钠试样2.5000g配成250mL溶液,取出25.00mL于碘量瓶中,加入10mL 2mol•L-1H2SO4和足量碘化钠(铬的还原产物为Cr3+),放于暗处5min,然后加入100mL水,加入3mL淀粉指示剂,用0.1200mol•L-1Na2S2O3标准溶液滴定(I2+2S2O32-═2I-+S4O62-).
①判断达到滴定终点的依据是:当滴加最后一滴硫代硫酸钠溶液时,溶液蓝色褪去,半分钟内不变色;
②若实验中共用去Na2S2O3标准溶液40.00ml,所得产品的中重铬酸钠的纯度(设整个过程中其它杂质不参与反应)83.84%.

①中涉及的主要反应有:
主反应:4FeO•Cr2O3+8Na2CO3+7O2$\frac{\underline{\;\;△\;\;}}{\;}$8Na2CrO4+2Fe2O3+8CO2
副反应:SiO2+Na2CO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2SiO3+CO2↑、Al2O3+Na2CO3$\frac{\underline{\;\;△\;\;}}{\;}$2NaAlO2+CO2↑
部分阳离子以氢氧化物形式完全沉淀时溶液的pH:
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Mg(OH)2 | Cr(OH)3 |
| 完全沉淀时溶液pH | 4.7 | 3.7 | 11.2 | 5.6 |
(1)“①”中反应是在回转窑中进行,反应时需不断搅拌,其作用是使反应物接触更充分,加快反应速率.
(2)“③”中调节pH至4.7,目的是除去溶液中的AlO2-、SiO32-.
(3)“⑤”中加硫酸酸化的目的是使CrO42-转化为Cr2O72-,请写出该平衡转化的离子方程式:2CrO42-+2H+?Cr2O72-+H2O.
(4)称取重铬酸钠试样2.5000g配成250mL溶液,取出25.00mL于碘量瓶中,加入10mL 2mol•L-1H2SO4和足量碘化钠(铬的还原产物为Cr3+),放于暗处5min,然后加入100mL水,加入3mL淀粉指示剂,用0.1200mol•L-1Na2S2O3标准溶液滴定(I2+2S2O32-═2I-+S4O62-).
①判断达到滴定终点的依据是:当滴加最后一滴硫代硫酸钠溶液时,溶液蓝色褪去,半分钟内不变色;
②若实验中共用去Na2S2O3标准溶液40.00ml,所得产品的中重铬酸钠的纯度(设整个过程中其它杂质不参与反应)83.84%.
17.用纯净的CaCO3与稀盐酸反应制CO2,实验过程记录如图所示.根据分析判断正确的是( ) 
0 157787 157795 157801 157805 157811 157813 157817 157823 157825 157831 157837 157841 157843 157847 157853 157855 157861 157865 157867 157871 157873 157877 157879 157881 157882 157883 157885 157886 157887 157889 157891 157895 157897 157901 157903 157907 157913 157915 157921 157925 157927 157931 157937 157943 157945 157951 157955 157957 157963 157967 157973 157981 203614

| A. | OE段表示反应速率最快 | |
| B. | EF段表示反应速率最快,收集的CO2最多 | |
| C. | FG段表示收集的CO2最多 | |
| D. | OG段表示随着时间的推移,反应速率逐渐增快 |


 如图为氨气溶于水的喷泉实验装置(图中固定装置均已略去).
如图为氨气溶于水的喷泉实验装置(图中固定装置均已略去).