9.下列能为人体提供能量的营养物质中,属于高分子化合物的是( )
| A. | 蔗糖 | B. | 油脂 | C. | 葡萄糖 | D. | 蛋白质 |
8.高锰酸钾是一种典型的强氧化剂,无论在实验室还是在化工生产中都有重要的应用.
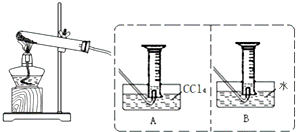
下图是实验室制备氯气并进行一系列相关实验的装置(夹持设备已略).

(1)制备氯气选用的药品为:高锰酸钾和浓盐酸,相应的离子方程式为:2MnO4-+16H++10Cl-=2 Mn2++5Cl2↑+8H2O.
(2)装置B的作用是除杂和安全瓶,监测实验进行时C中可能发生堵塞,请写出发生堵塞时B中的现象锥形瓶中液面下降,长颈漏斗中液面上升.
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中I、II、III依次放入c.(选a或b或c)
(4)设计装置D、E的目的是比较氯、溴、碘的非金属性.当向D中缓缓通入足量氯气时,可以看到无色溶液逐渐变为红棕色,说明氯的非金属性大于溴.打开活塞,将D中的少量溶液加入E中,振荡E.观察到的现象是E中溶液分为两层,上层(苯层)为紫红色.该现象不能(填“能”或“不能”)说明溴的非金属性强于碘,原因是过量的Cl2也可将I-氧化为I2.
下图是实验室制备氯气并进行一系列相关实验的装置(夹持设备已略).

(1)制备氯气选用的药品为:高锰酸钾和浓盐酸,相应的离子方程式为:2MnO4-+16H++10Cl-=2 Mn2++5Cl2↑+8H2O.
(2)装置B的作用是除杂和安全瓶,监测实验进行时C中可能发生堵塞,请写出发生堵塞时B中的现象锥形瓶中液面下降,长颈漏斗中液面上升.
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中I、II、III依次放入c.(选a或b或c)
| a | b | c | |
| I | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
| II | 碱石灰 | 浓硫酸 | 无水氯化钙 |
| III | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
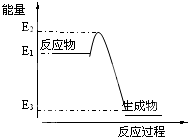
4.下列有关化学反应与能量变化的说法正确的是( )

| A. | 甲烷的燃烧热△H=-890.3kJ•mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+$\frac{3}{2}$O2(g)=CO(g)+2H2O(g)△H=-890.3kJ•mol-1 | |
| B. | 相同条件下,氢气和氧气反应生成液态水比生成等量的气态水所放出的热量少 | |
| C. | 根据图金刚石在一定条件下转化成石墨提供的信息,可知生成物比反应物稳定,向外界放出的热量为E2-E3 | |
| D. | 同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的△H相同 |
3.在甲烧杯中放入盐酸,乙烧杯中放入醋酸,两种溶液的体积和pH都相等,向两烧杯中同时加入质量不等的锌粒,反应结束后得到等量的氢气.下列说法正确的是( )
| A. | 两烧杯中生成氢气的平均速率甲大于乙 | |
| B. | 甲烧杯中的酸过量 | |
| C. | 甲烧杯中放入锌的质量比乙烧杯中放入锌的质量大 | |
| D. | 反应开始后乙烧杯中的c(H+)始终比甲烧杯中的c(H+)小 |
2.用铜做电极,电解某浓度的AgNO3和Cu(NO3)2的混合溶液,一段时间后,阴极上析出1.6gCu时,不考虑溶液体积变化,则下列叙述中正确的是( )
| A. | 电路中流过0.05mol电子 | B. | 溶液中c(Cu2+)降低 | ||
| C. | 电解质溶液质量减少 | D. | 阳极铜消耗了1.6g |
1.用石墨电极电解下列足量的各物质水溶液一段时间后,假如通过的电量相同,则产生气体的物质的量最少的是( )
0 157762 157770 157776 157780 157786 157788 157792 157798 157800 157806 157812 157816 157818 157822 157828 157830 157836 157840 157842 157846 157848 157852 157854 157856 157857 157858 157860 157861 157862 157864 157866 157870 157872 157876 157878 157882 157888 157890 157896 157900 157902 157906 157912 157918 157920 157926 157930 157932 157938 157942 157948 157956 203614
| A. | CuSO4 | B. | Na2SO4 | C. | CuCl2 | D. | NaCl |
 X、Y、Z为三种常见的单质,Z为绿色植物光合作用后的产物之一,A、B为常见的化合物.它们在一定条件下可以发生如图所示的转化关系(均不是在溶液中进行的反应)以下每空中填入一种即可).
X、Y、Z为三种常见的单质,Z为绿色植物光合作用后的产物之一,A、B为常见的化合物.它们在一定条件下可以发生如图所示的转化关系(均不是在溶液中进行的反应)以下每空中填入一种即可). 和
和 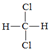 ④CH3CH2CH3和CH3CH3 ⑤氕和氘 ⑥CH3CH2CH2CH2CH3和CH3C(CH3)3
④CH3CH2CH3和CH3CH3 ⑤氕和氘 ⑥CH3CH2CH2CH2CH3和CH3C(CH3)3