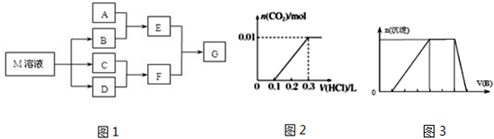
19.某化学兴趣小组制取氯酸钾和氯水并进行有关探究实验.实验一制取氯酸钾和氯水利用如图1所示的实验装置进行实验.

(1)制取实验结束后,取出B中试管冷却结晶、过滤、洗涤.该实验操作过程需要的玻璃仪器有胶头滴管、烧杯外,还需要的玻璃仪器是漏斗、玻璃棒.
(2)若对调B和C装置的位置,能(填“能”或“不能”)提高B中氯酸钾的产率.
实验二 氯酸钾与碘化钾反应的探究
(3)在不同条件下KClO3可将KI氧化为I2或KIO3.该小组设计了系列实验研究反应条件对反应产物的影响,其中系列a实验的记录表如下(实验在室温下进行):
①系列a实验的实验目的是研究反应体系中硫酸浓度对反应产物的影响.
②设计1号试管实验的作用是硫酸浓度为0的对照实验.
③若2号试管实验现象为“黄色溶液”,取少量该溶液加入淀粉溶液显蓝色;假设氧化产物唯一,还原产物为KCl,则此反应的离子方程式为ClO3-+6I-+6H+=Cl-+3I2+3H2O.
实验三 测定饱和氯水中氯元素的总量
(4)该小组设计的实验方案为:使用图2装置,加热15.0ml饱和氯水试样,测定产生气体的体积.此方案是否可行否(填“是”或“否”)
(5)另一小组研究出的方案是,量取一定量的试样,加入足的H2O2溶液,加热除去过量的H2O2,冷却,再加入足量的硝酸银溶液,还需进行的操作是过滤、洗涤、干燥、称量沉淀质量
已知:次氯酸或氯水可被SO2、H2O2、FeCl2等物质还原成Cl-.

(1)制取实验结束后,取出B中试管冷却结晶、过滤、洗涤.该实验操作过程需要的玻璃仪器有胶头滴管、烧杯外,还需要的玻璃仪器是漏斗、玻璃棒.
(2)若对调B和C装置的位置,能(填“能”或“不能”)提高B中氯酸钾的产率.
实验二 氯酸钾与碘化钾反应的探究
(3)在不同条件下KClO3可将KI氧化为I2或KIO3.该小组设计了系列实验研究反应条件对反应产物的影响,其中系列a实验的记录表如下(实验在室温下进行):
| 试管编号 | 1 | 2 | 3 | 4 |
| 0.20mol•L-1KI/mL | 1.0 | 1.0 | 1.0 | 1.0 |
| KClO3(s)/g | 0.10 | 0.10 | 0.10 | 0.10 |
| 6.0mol•L-1H2SO4/mL | 0 | 3.0 | 6.0 | 9.0 |
| 蒸馏水 | 9.0 | 6.0 | 3.0 | 0 |
| 实验现象 |
②设计1号试管实验的作用是硫酸浓度为0的对照实验.
③若2号试管实验现象为“黄色溶液”,取少量该溶液加入淀粉溶液显蓝色;假设氧化产物唯一,还原产物为KCl,则此反应的离子方程式为ClO3-+6I-+6H+=Cl-+3I2+3H2O.
实验三 测定饱和氯水中氯元素的总量
(4)该小组设计的实验方案为:使用图2装置,加热15.0ml饱和氯水试样,测定产生气体的体积.此方案是否可行否(填“是”或“否”)
(5)另一小组研究出的方案是,量取一定量的试样,加入足的H2O2溶液,加热除去过量的H2O2,冷却,再加入足量的硝酸银溶液,还需进行的操作是过滤、洗涤、干燥、称量沉淀质量
已知:次氯酸或氯水可被SO2、H2O2、FeCl2等物质还原成Cl-.
18.在通风橱中进行下列实验:
下列说法中不正确的是( )
| 步骤 | 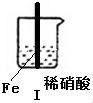 |  | |
| 现象 | Fe表面产生大量无色气泡,液面上方变为红棕色 | Fe表面产生少量红棕色气泡后,迅速停止 | Fe、Cu接触后,其表面产生红棕色气泡 |
| A. | Ⅰ中气体由无色变红棕色的化学方程式为:2NO+O2═2NO2 | |
| B. | Ⅱ中的现象说明Fe表面形成致密的氧化层,阻止Fe进一步反应 | |
| C. | 针对Ⅲ中现象,在Fe、Cu之间连接电流计,可判断Fe是否被氧化 | |
| D. | 对比Ⅰ、Ⅱ中现象,说明稀HNO3的氧化性强于浓HNO3 |
16.表给出了五种元素的相关信息,其中A、B、C、D为短周期元素.根据以下信息填空:
(1)C与A形成的气态化合物16g能和C与B形成的另一无色气态化合物(这两种化合物分子中原子个数比皆为1:2)发生反应生成无毒物质和液态水,并放出284kg的热量,写出上述热化学反应方程式:2 N2H4(g)+N2O4(g)=3N2(g)+4H2O(l)△H=-1136kJ/mol.
(2)化合物X是元素D的氢化物,X在水中的电离方程为H2S?H++HS-;元素E在元素周期表中的位置是第四周期第Ⅷ族.
| 元素 | 相关信息 |
| A | 在常温、常压下,其单质是气体,随着人类对环境的认识和要求的提高,它将成为备受青睐的清洁燃料 |
| B | 工业上通过分离液态空气获得其单质,其某种同素异形体是保护地球地表环境的重要屏障 |
| C | 植物生长三要素之一,它能形成多种氧化物,其中一种是早期医疗中使用的麻醉剂 |
| D | 室温下其单质为淡黄色粉末状固体,加热易熔化.该单质在氧气中燃烧,发出明亮的蓝紫色火焰 |
| E | 它在地壳中储量丰富,是人体不可缺少的微量元素之一.其单质为银白色固体,是工农业生产中不可或缺的金属材料,常用于机械制备、建筑等行业 |
(2)化合物X是元素D的氢化物,X在水中的电离方程为H2S?H++HS-;元素E在元素周期表中的位置是第四周期第Ⅷ族.
14.下列化学反应的离子方程式不正确的是( )
| A. | 向NaHSO3溶液中加入NaHSO4溶液:HSO3-+H+═H2O+SO2↑ | |
| B. | 0.01 mol•L-1 NH4Al(SO4)2溶液与0.02 mol•L-1 Ba(OH)2溶液等体积混合:Al3++2Ba2++4OH-+2SO42-═2BaSO4↓+AlO2-+2H2O | |
| C. | 小苏打溶液与乙酸溶液混合 HCO3-+CH3COOH═CH3COO-+H2O+CO2↑ | |
| D. | AlCl3溶液中加入过量氨水:Al3++3NH3•H2O═Al(OH)3↓+3NH4+ |
13.下列关于物质或离子检验的叙述正确的是( )
| A. | 向某溶液中滴加氯水,再滴加KSCN溶液,若溶液变成血红色,则原溶液中一定有Fe2+ | |
| B. | 钾元素焰色反应的操作是:将铂丝放在稀盐酸中洗涤后灼烧至无色,然后再用铂丝蘸取固体氯化钾,进行灼烧,直接观察火焰颜色 | |
| C. | 向某溶液中滴加氯化钡溶液,产生白色沉淀,再滴加足量稀硝酸,依然有白色固体,说明原溶液含有SO42- | |
| D. | 向某黄色溶液中加入淀粉溶液,若溶液变蓝色,则原溶液中含有I2 |
12.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 1L 0.1mol•L-1FeCl3溶液中含有的Fe3+离子数目为0.1NA | |
| B. | 室温下,1L pH=13的NaOH溶液中,由水电离的OH-离子数目为0.1NA | |
| C. | 5NH4NO3$\frac{\underline{\;\;△\;\;}}{\;}$2HNO3+4N2↑+9H2O反应中,生成28g N2时,转移的电子数目为3.75NA | |
| D. | 常温下,2.24LCl2完全与NaOH溶液反应,转移的电子数目一定为0.1NA |
11.化学反应中会出现“一种物质过量,另一种物质仍不能完全反应”的特殊情况.下列反应中属于这种情况的是( )
①过量稀硫酸与块状石灰石;
②过量的氢气与少量氮气在催化剂存在下充分反应;
③过量稀硝酸与银反应;
④过量铜与浓硫酸;
⑤浓盐酸与过量的MnO2
⑥过量的锌与18mol/L的硫酸反应.
①过量稀硫酸与块状石灰石;
②过量的氢气与少量氮气在催化剂存在下充分反应;
③过量稀硝酸与银反应;
④过量铜与浓硫酸;
⑤浓盐酸与过量的MnO2
⑥过量的锌与18mol/L的硫酸反应.
| A. | ③④⑥ | B. | ②③⑤ | C. | ①②④⑤ | D. | ①②③④⑤⑥ |
10.下列指定微粒的数目相等的是( )
0 157753 157761 157767 157771 157777 157779 157783 157789 157791 157797 157803 157807 157809 157813 157819 157821 157827 157831 157833 157837 157839 157843 157845 157847 157848 157849 157851 157852 157853 157855 157857 157861 157863 157867 157869 157873 157879 157881 157887 157891 157893 157897 157903 157909 157911 157917 157921 157923 157929 157933 157939 157947 203614
| A. | 等物质的量的CaCl2和CaO2含有的离子数 | |
| B. | 等质量的水与重水含有的电子数 | |
| C. | 同温、同压同体积的CO和NO含有的质子数 | |
| D. | 等物质的量的铁和铝分别与足量氯气完全反应时转移的电子数 |