10.假设12C的相对原子质量为24,则下列推断中,不正确的是( )
| A. | 标准状况时11.2LO2的质量为32g | B. | 16O的相对原子质量为32 | ||
| C. | 44gCO2和28gCO含有相同的分子数 | D. | 标准状况时44gCO2的体积是22.4L |
7.用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,44.8L苯中所含分子数为2NA | |
| B. | 标准状况下,11.2L的12C16O和14N2混合气体所含中子数和原子数的差值为6NA | |
| C. | 常温下,1L pH=14的NaOH溶液中由水电离出的OH-个数为NA | |
| D. | 2mol Cl2通入足量的水中转移电子数目为2NA |
6.将200mL 0.1mol•L-1 Na2CO3溶液与含1.71gBa(OH)2的溶液混合后,为使混合液呈中性,需再加入1mol•L-1盐酸的体积为( )
| A. | 30mL | B. | 40mL | C. | 50mL | D. | 60mL |
4.钴的氧化物广泛应用于磁性材料及超导材料等领域.取0.2mol Co5O6(其中结合钴的化合价为+2、+3),用足量浓盐酸溶解,得到CoCl2溶液和4.48L(标准状况)黄绿色气体,则原化合物中+2价Co的物质的量为( )
| A. | 0.2mol | B. | 0.4mol | C. | 0.6mol | D. | 0.8mol |
3.下列反应属于氧化还原反应的是( )
①Na2O2+2H2O═2NaOH+H2O2
②IBr+H2O═HIO+HBr
③Cr2O72-+4H2O2+2H+═2CrO5+5H2O(CrO5的结构为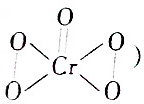 )
)
①Na2O2+2H2O═2NaOH+H2O2
②IBr+H2O═HIO+HBr
③Cr2O72-+4H2O2+2H+═2CrO5+5H2O(CrO5的结构为
 )
)| A. | ①②③ | B. | ② | C. | ③ | D. | 都不是 |
2.下列离子方程式表达不正确的是( )
| A. | 在硫酸亚铁溶液中通入氧气:4Fe2++O2+4H+=4Fe3++2H2O | |
| B. | 用0.3mol/L的氯化铵溶液除去氢氧化铝中少量的氢氧化镁:Mg(OH)2+2NH4+=Mg2++2NH3•H2O | |
| C. | 向1mol明矾的水溶液当中加入氢氧化钡,当沉淀的质量最大时离子方程式科表示为:Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2H2O | |
| D. | 酸性高锰酸钾和过氧化氢制取少量氧气:4MnO4-+4H2O2+12H+=4Mn 2++7O2↓+10H2O |
1.在氯化铁和氯化铜的混合溶液中,加入过量铁粉,完全反应后过滤,所得固体的质量与所加铁粉的质量相等,则原混合液中氯化铁和氯化铜的物质的量浓度之比是( )
0 157747 157755 157761 157765 157771 157773 157777 157783 157785 157791 157797 157801 157803 157807 157813 157815 157821 157825 157827 157831 157833 157837 157839 157841 157842 157843 157845 157846 157847 157849 157851 157855 157857 157861 157863 157867 157873 157875 157881 157885 157887 157891 157897 157903 157905 157911 157915 157917 157923 157927 157933 157941 203614
| A. | 7:2 | B. | 2:7 | C. | 1:2 | D. | 2:1 |
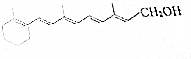 维生素A(见图)是一切健康上皮组织必需的物质,缺乏维生素A时会引起儿童发育不良,导致夜盲症、皮肤干燥等多种病症.
维生素A(见图)是一切健康上皮组织必需的物质,缺乏维生素A时会引起儿童发育不良,导致夜盲症、皮肤干燥等多种病症.