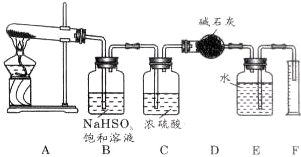
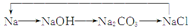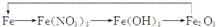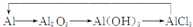20.下表中实验操作、现象和所得出的结论正确的是( )
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 用激光笔照射鸡蛋白水溶液 | 有丁达尔效应 | 鸡蛋白分子直径介于1nm~100nm |
| B | 向某氯化亚铁溶液中加入Na2O2粉末 | 出现红褐色沉淀 | 说明原氯化亚铁已氧化变质 |
| C | 碳酸盐X加热分解,产生的气体通入酸化的BaCl2溶液 | 产生白色沉淀 | X可能是NaHCO3 |
| D | 湿润的KI淀粉试纸靠近气体Y | 试纸变蓝 | Y一定是Cl2 |
| A. | A | B. | B | C. | C | D. | D |
19.下列说法中正确的是( )
| A. | 干冰、浓硫酸都是电解质 | |
| B. | Na2O2晶体中既含有离子键又含有共价键 | |
| C. | CaO,Fe2O3、Al2O3既属于碱性氧化物,又属于离子化合物 | |
| D. | 含同一元素的不同化合物,该元素的化合价越高,其氧化性越强 |
15.某溶液可能含有Cl-、SO42-、CO32-、NH4+、Fe2+、Al3+和K+.取该溶液100mL,加入过量NaOH溶液,加热,得到0.02mol气体,同时产生沉淀;过滤、洗涤、灼烧,得到1.6g红棕色固体;向上述滤液中加入足量BaCl2溶液,得到4.66g不溶于盐酸的沉淀.由此可知原溶液中( )
| A. | 至少存在4种离子 | |
| B. | Cl-一定存在,且c(Cl )≥0.4 mol/L | |
| C. | SO42-、NH4+,一定存在,Cl-可能不存在 | |
| D. | CO32-、Al3+一定不存在,K+可能存在 |
14.下列类比分析结果正确的是( )
| A. | Fe3O4根据化合价规律可表示为FeO•Fe2O3,则Pb3O4也可表示为PbO•Pb2O3 | |
| B. | CaC2能水解:CaC2+2H2O=Ca(OH)2+C2H2↑,则Al4C3也能水解:Al4C3+12H2O=4A1(OH)3↓+3CH4↑ | |
| C. | Cl2与Fe加热生成FeCl3,则I2与Fe加热生成FeI3 | |
| D. | SO2通入BaCl2溶液不产生沉淀,则SO2通入Ba(NO3)2溶液也不产生沉淀 |
12.将一定量的Fe、Fe2O3 CuO的混合物放入体积为100mL、浓度为2.2mol•L-1的H2SO4溶液中,充分反应后,生成气体896mL(标准状况),得到不溶固体1.28g.过滤后,滤液中的金属离子只有Fe2+(假设滤液体积仍为l00mL).向滤液中滴加2mol•L-1NaOH 溶液,直至40mL时开始出现沉淀.则未滴加NaOH溶液前滤液中FeSO4的物质的量浓度为( )
| A. | 2mol•L-1 | B. | 1.8 mol•L-1 | C. | 1.4 mol•L-1 | D. | 无法计算 |
11.下列各组离子中,在给定条件下能够大量共存的是( )
0 157742 157750 157756 157760 157766 157768 157772 157778 157780 157786 157792 157796 157798 157802 157808 157810 157816 157820 157822 157826 157828 157832 157834 157836 157837 157838 157840 157841 157842 157844 157846 157850 157852 157856 157858 157862 157868 157870 157876 157880 157882 157886 157892 157898 157900 157906 157910 157912 157918 157922 157928 157936 203614
| A. | 通入足量CO2后的溶液中:Na+、SiO32-、CH3COO-、CO32- | |
| B. | 中性溶液中:Fe3+、MnO4-、SO42-、K+ | |
| C. | 酸性溶液中:Na+、ClO-、SO42-、I- | |
| D. | $\frac{c({H}^{+})}{c(O{H}^{-})}$=1012的溶液中:NH4+、Al3+、NO3-、Cl- |