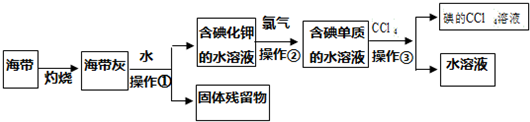
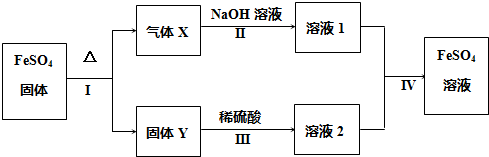
20.关于吸热反应的说法正确的是( )
| A. | 凡需加热的反应一定是吸热反应 | |
| B. | 反应物的总能量比生成物的总能量大 | |
| C. | 氢氧化钠与盐酸的反应属于吸热反应 | |
| D. | CO2与CaO化合是放热反应,则CaCO3分解是吸热反应 |
17.在如图所示的8个装置中,属于原电池的是( )


| A. | ②④ | B. | ③④⑤ | C. | ①④⑧ | D. | ②④⑥⑦ |
16.设阿伏伽德罗常数为NA,则下列说法正确的是( )
0 157740 157748 157754 157758 157764 157766 157770 157776 157778 157784 157790 157794 157796 157800 157806 157808 157814 157818 157820 157824 157826 157830 157832 157834 157835 157836 157838 157839 157840 157842 157844 157848 157850 157854 157856 157860 157866 157868 157874 157878 157880 157884 157890 157896 157898 157904 157908 157910 157916 157920 157926 157934 203614
| A. | 1.5g甲基(-CH3)所含有的电子数是NA | |
| B. | 14g乙烯和丙烯的混合物中含有原子的数目为NA | |
| C. | 常温常压下,1molCnH2n+2中所含有的共价键数目为(3n+1)NA | |
| D. | 标准状况下,1L戊烷充分燃烧后生成的气态产物的分子数为5/22.4NA |
 .
.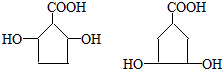 .
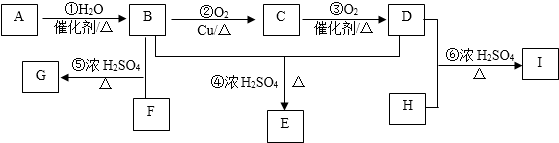
.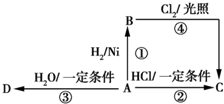 某烃A是有机化学工业的基础原料,其产量可以用来衡量一个国家的石油化工发展水平,A还是一种植物生长调节剂,A可发生如图所示的一系列化学反应,其中①②③属于同种反应类型.
某烃A是有机化学工业的基础原料,其产量可以用来衡量一个国家的石油化工发展水平,A还是一种植物生长调节剂,A可发生如图所示的一系列化学反应,其中①②③属于同种反应类型.