10.某学生配制的1mol/L-1的NaOH溶液,实际浓度偏高的原因可能是( )
| A. | 洗净的容量瓶中残留少量的蒸馏水 | B. | 溶解NaOH的烧杯未洗净 | ||
| C. | 称量NaOH时使用称量纸 | D. | 定容时俯视刻度线 |
9.下列操作中不属于萃取的是( )
| A. | 从青蒿中提取青蒿素 | B. | 从溴水中提取溴单质 | ||
| C. | 浸泡药酒 | D. | 海水淡化 |
5.电子表和电子计算器的电源常用微型银锌原电池,其电极分别为Ag2O和Zn,电解质溶液为KOH溶液,放电时锌极上的电极反应式为:Zn+2OH--2e-═Zn(OH)2;氧化银电极上的反应式为:Ag2O+H2O+2e-═2Ag+2OH-,总反应式为:Ag2O+H2O+Zn═Zn(OH)2+2Ag.下列说法正确的是( )
| A. | 锌是负极,发生氧化反应 | |
| B. | 锌的质量减少6.5g,外电路中通过0.4mol电子 | |
| C. | 溶液中OH-向正极移动,K+、H+向负极移动 | |
| D. | 随着电极反应的不断进行,电解质溶液中n(OH-)减小 |
4.下列各离子组可在同一溶液中大量共存,且形成无色溶液的是( )
| A. | K+、Na+、OH-、NO3- | B. | Cu2+、Ba2+、Cl-、NO3- | ||
| C. | Na+、Mg2+、OH-、SO42- | D. | Fe2+、H+、NO3-、ClO- |
3.室温下,下列溶液中粒子浓度关系不正确的是( )
0 157737 157745 157751 157755 157761 157763 157767 157773 157775 157781 157787 157791 157793 157797 157803 157805 157811 157815 157817 157821 157823 157827 157829 157831 157832 157833 157835 157836 157837 157839 157841 157845 157847 157851 157853 157857 157863 157865 157871 157875 157877 157881 157887 157893 157895 157901 157905 157907 157913 157917 157923 157931 203614
| A. | pH=1 的 NaHSO4溶液:c(H+)=c(SO42-)+c(OH-) | |
| B. | 0.1 mol•L-1NaHCO3溶液与 0.1 mol•L-1NaOH 溶液等体积混合,所得溶液中:c(Na+)>c(CO32-)>c(OH-)>c(HCO3-) | |
| C. | CH3COONa 和 CaCl2混合溶液:c(Na+)+c(Ca2+)=c(CH3COO-)+c(CH3COOH)+2c(Cl-) | |
| D. | 含等物质的量的 NaHC2O4和 Na2C2O4的溶液:2 c(Na+)=3c(HC2O4-)+3c(C2O42-)+3c(H2C2O4) |
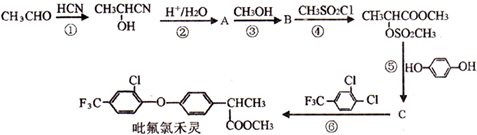
 .
. .
.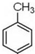 制备高分子化合物
制备高分子化合物 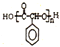 的合成路线流程图(无机试剂任选),合成流程示意图如下:CH3CH2$→_{170℃}^{H_{2}SO_{4}}$CH2$→_{催化剂△}^{H_{2}}$CH3CH3.
的合成路线流程图(无机试剂任选),合成流程示意图如下:CH3CH2$→_{170℃}^{H_{2}SO_{4}}$CH2$→_{催化剂△}^{H_{2}}$CH3CH3. .
.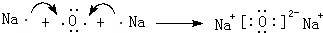 .
.

 ;
;

 .
. ,该物质在NaOH水溶液中加热反应时的化学方程式为
,该物质在NaOH水溶液中加热反应时的化学方程式为 +5NaOH$→_{△}^{H_{2}O}$
+5NaOH$→_{△}^{H_{2}O}$ +HOCH2CH2OH+Na2CO3+NaCl+2H2O.
+HOCH2CH2OH+Na2CO3+NaCl+2H2O.

 )
) .由甲苯生成甲的反应类型是取代反应.
.由甲苯生成甲的反应类型是取代反应. +HOCH2CH2Cl$→_{△}^{浓硫酸}$
+HOCH2CH2Cl$→_{△}^{浓硫酸}$ +H2O.
+H2O. .
. .
. .
.