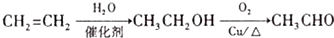12.下列反应的离子方程式正确的是( )
| A. | 氯化镁溶液中加氨水:Mg2++2NH3•H2O=Mg(OH)2↓+2NH4+ | |
| B. | 钠与水反应:Na+2H2O=Na++2OH-+H2↑ | |
| C. | 稀硫酸与氢氧化钡溶液混合:H++SO42-+Ba2++OH-=BaSO4↓+H2O | |
| D. | 碳酸钙溶于醋酸溶液:CaCO3+2H+=Ca2++CO2↑+H2O |
11.根据图,下列判断中正确的是( )
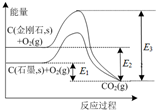

| A. | 石墨与O2生成CO2的反应是吸热反应 | |
| B. | 等量金刚石和石墨完全燃烧,金刚石放出热量更多 | |
| C. | 从能量角度看,金刚石比石墨更稳定 | |
| D. | 金刚石转化为石墨需要吸收的能量为E3-E2 |
10.下列物质的水溶液因水解而显酸性的是( )
| A. | KNO3 | B. | Fe2(SO4)3 | C. | Na2CO3 | D. | H2SO4 |
9.常温下能与水反应的非金属单质是( )
| A. | Na | B. | C | C. | Cl2 | D. | NH3 |
8.下列仪器中一般不能用作反应容器的是( )
| A. |  | B. |  | C. | 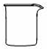 | D. | 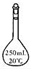 |
7.已知:A是石油裂解气的主要成份,A的产量通常用来衡量一个国家的石油化工水平. 现以A为主要原料合成乙酸乙酯,其合成路线如图1所示.
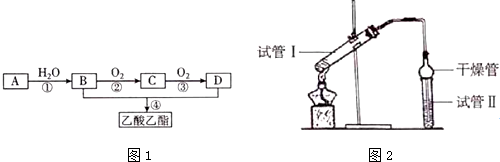
(1)有机物D中官能团的名称为羧基,①、④的反应类型分别为加成反应、酯化反应或取代反应.
(2)反应④的化学方程式为CH3CH2OH+CH3COOH$?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O.
(3)乙酸乙酯是重要的有机合成中间体,广泛应用于化学工业.实验室利用图2的装罝制备乙酸乙酯.
①与教材采用的实验装置不同,此装置中采用了球形干燥管,其作用是:防倒吸.
②试管Ⅱ中加入的试剂是饱和Na2CO3溶液,其作用是:吸收乙酸和乙醇,降低乙酸乙酯的溶解度.
③为了证明浓硫酸在该反应中起到了催化剂和吸水剂的作用,某同学利用该装置进行了以下4 个实验.实验开始先用酒精灯微热3min,再加热使之微微沸腾3min.实验结束后充分振荡小试管Ⅱ,再测其中有机层的厚度,实验记录如下:
实验D的目的是与实验C相对照,证明H+对酯化反应具有催化作用,则进行实验D时应加入2 mL6mol•L-1的盐酸.分析实验A和实验C的数据,可以推断出浓H2SO4的吸水(填“催化”或“吸水”)作用提高了乙酸乙酯的产率.
(4)乙醇在一定条件下可转化为有机物E,E的相对分子质里为74,其分子中碳、氢的质量分数分别为64.9%、13.5%,其余为氧.求E的化学式C原子个数=$\frac{74×64.9%}{12}$≈4、H原子个数=$\frac{74×13.5%}{1}$≈10,则O原子个数=$\frac{74-12×4-1×10}{16}$=1,则C、H、O原子个数之比=4:10:1,则E的化学式为C4H10O(需写出计算过程).

(1)有机物D中官能团的名称为羧基,①、④的反应类型分别为加成反应、酯化反应或取代反应.
(2)反应④的化学方程式为CH3CH2OH+CH3COOH$?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O.
(3)乙酸乙酯是重要的有机合成中间体,广泛应用于化学工业.实验室利用图2的装罝制备乙酸乙酯.
①与教材采用的实验装置不同,此装置中采用了球形干燥管,其作用是:防倒吸.
②试管Ⅱ中加入的试剂是饱和Na2CO3溶液,其作用是:吸收乙酸和乙醇,降低乙酸乙酯的溶解度.
③为了证明浓硫酸在该反应中起到了催化剂和吸水剂的作用,某同学利用该装置进行了以下4 个实验.实验开始先用酒精灯微热3min,再加热使之微微沸腾3min.实验结束后充分振荡小试管Ⅱ,再测其中有机层的厚度,实验记录如下:
| 实验编号 | 试管I中试剂 | 试管Ⅱ中有机层的厚度/cm |
| A | 3mL乙醇、2mL乙酸、2mL 18mol•L-1浓硫酸 | 3.0 |
| B | 3mL乙醇、2mL乙酸 | 0.1 |
| C | 3mL 乙醇、2mL 乙酸 2mL3mol•L-1H2SO4 | 0.6 |
| D | 3mL乙醇、2mL乙酸、盐酸 | 0.6 |
(4)乙醇在一定条件下可转化为有机物E,E的相对分子质里为74,其分子中碳、氢的质量分数分别为64.9%、13.5%,其余为氧.求E的化学式C原子个数=$\frac{74×64.9%}{12}$≈4、H原子个数=$\frac{74×13.5%}{1}$≈10,则O原子个数=$\frac{74-12×4-1×10}{16}$=1,则C、H、O原子个数之比=4:10:1,则E的化学式为C4H10O(需写出计算过程).
5.近两年流行喝果醋,苹果醋是一种由苹果发酵而成的具有解毒、降脂、减肥和止泻等明显药效的健康食品.苹果酸(a-羟基丁二酸)是这种饮料中的主要酸性物质,苹果酸的结构简式为: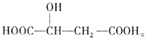 下列说法不正确的是( )
下列说法不正确的是( )
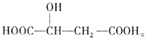 下列说法不正确的是( )
下列说法不正确的是( )| A. | 苹果酸在一定条件下能与乙醇发生反应 | |
| B. | 苹果酸在一定条件下能发生催化氧化反应 | |
| C. | 苹果酸在一定条件下能与乙酸发生反应 | |
| D. | 1mol苹果酸与Na2CO3溶液反应最多消耗3mol Na2CO3 |
4.下列实验能获得成功的是( )
| A. | 用溴水可鉴别苯、乙醇、苯乙烯 | |
| B. | 加浓溴水,然后过滤可除去苯中的少量乙烯 | |
| C. | 用酸性KMnO4溶液可除去甲烷中的乙烯 | |
| D. | 用新制的Cu(OH)2悬浊液可鉴别乙醇、乙醛、乙酸 |
3.在l℃时,10mL0.4mol•L-1H2O2溶液发生催化分解:2H2O2 $\frac{\underline{\;催化剂\;}}{\;}$ 2H2O+O2↑,不同时刻测得生成O2的体积(已折算为标准状况)如下表:
下列叙述不正确的是(溶液体积变化忽略不计)( )
0 157706 157714 157720 157724 157730 157732 157736 157742 157744 157750 157756 157760 157762 157766 157772 157774 157780 157784 157786 157790 157792 157796 157798 157800 157801 157802 157804 157805 157806 157808 157810 157814 157816 157820 157822 157826 157832 157834 157840 157844 157846 157850 157856 157862 157864 157870 157874 157876 157882 157886 157892 157900 203614
| t/min | 0 | 2 | 4 | 6 |
| V( 02 )/mL | 0.0 | 9.9 | 17.2 | 22.4 |
| A. | 0-2min的平均反应速率比4-6min快 | |
| B. | 0-6min 的平均反应速率v( H2O2)=3.3 x 10-2 moL-1•min-1 | |
| C. | 反应至 6min 时,c( H2O2)=0.3mol•L-1 | |
| D. | 反应至6min时,H2O2分解了 50% |
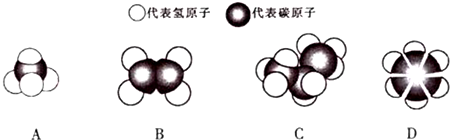
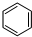 +3H2$\stackrel{催化剂}{→}$
+3H2$\stackrel{催化剂}{→}$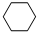 .
. .
. 路线流程图(无机试剂任选).合成路线流程图示例如下:
路线流程图(无机试剂任选).合成路线流程图示例如下: