2. 如图所示装置可用于( )
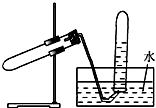
如图所示装置可用于( )
 如图所示装置可用于( )
如图所示装置可用于( )| A. | 加热NaHCO3制CO2 | B. | 用Cu和浓HNO3反应制NO2 | ||
| C. | 用Zn与稀硫酸反应制H2 | D. | 用NaCl与浓H2SO4加热制HCl |
1.100mL6mol/LH2S04与过量锌粉反应,在一定温度下,为了减缓反应进行的速率,但又不影响生成氢气的总量,可向反应物中加入适量的( )
| A. | 硫酸锌溶液 | B. | 氢氧化钠固体 | C. | 碳酸钠固体 | D. | 硫酸铜固体 |
20.决定化学反应在速率的主要因素是( )
| A. | 反应物的性质 | B. | 反应温度 | C. | 浓度 | D. | 压强 |
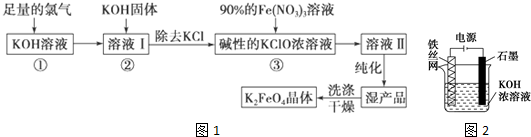
16.硼镁泥是一种工业废料,主要成份是MgO(占40%),还有CaO、MnO、Fe2O3、FeO、Al2O3、SiO2等杂质.以硼镁泥为原料制取的硫酸镁,可用于印染、造纸、医药等工业.从硼镁泥中提取MgSO4•7H2O的流程如图:
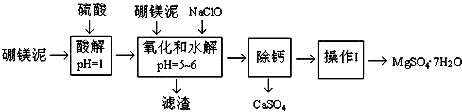
根据题意回答下列问题:
(1)在酸解过程中,想加快酸解速率,请提出两种可行的措施升温、把硼镁泥粉碎、搅拌等.
(2)滤渣的主要成份除含有Fe(OH)3、Al(OH)3、MnO2外,还有SiO2.
(3)加入的NaClO可与Mn2+反应产生MnO2沉淀,该反应的离子方程式是Mn2++ClO-+H2O═MnO2↓+2H++Cl-.在调节pH、发生水解之前,还有一种离子也会被NaClO氧化,该反应的离子方程式为2Fe2++ClO-+2H+═2Fe3++Cl-+H2O.
(4)为了检验滤液中Fe3+是否被除尽,可选用的试剂是取少量滤液,向其中加入硫氰化钾溶液,如果溶液不变红色,说明滤液中不含Fe3+;如果溶液变红色,说明滤液中含Fe3+.
A.KSCN B.淀粉-KI溶液 C.H2O2 D.KMnO4稀溶液
(5)已知MgSO4、CaSO4的溶解度如表:
“除钙”是将MgSO4和CaSO4混合溶液中的CaSO4除去,根据上表数据,简要说明除钙的操作步骤蒸发浓缩(结晶)、趁热过滤.
(6)现有l.60t硼镁泥,生产MgSO4•7H2O,若生产过程的产率为50%,则能生产出MgSO4•7H2O产品1.97t (计算结果保留三位有效数字).

根据题意回答下列问题:
(1)在酸解过程中,想加快酸解速率,请提出两种可行的措施升温、把硼镁泥粉碎、搅拌等.
(2)滤渣的主要成份除含有Fe(OH)3、Al(OH)3、MnO2外,还有SiO2.
(3)加入的NaClO可与Mn2+反应产生MnO2沉淀,该反应的离子方程式是Mn2++ClO-+H2O═MnO2↓+2H++Cl-.在调节pH、发生水解之前,还有一种离子也会被NaClO氧化,该反应的离子方程式为2Fe2++ClO-+2H+═2Fe3++Cl-+H2O.
(4)为了检验滤液中Fe3+是否被除尽,可选用的试剂是取少量滤液,向其中加入硫氰化钾溶液,如果溶液不变红色,说明滤液中不含Fe3+;如果溶液变红色,说明滤液中含Fe3+.
A.KSCN B.淀粉-KI溶液 C.H2O2 D.KMnO4稀溶液
(5)已知MgSO4、CaSO4的溶解度如表:
| 温度/℃ | 40 | 50 | 60 | 70 |
| MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
| CaSO4 | 0.210 | 0.207 | 0.201 | 0.193 |
(6)现有l.60t硼镁泥,生产MgSO4•7H2O,若生产过程的产率为50%,则能生产出MgSO4•7H2O产品1.97t (计算结果保留三位有效数字).
14.仅用下表提供的仪器(夹持仪器和试剂任选)不能实现相应实验目的是( )
| 选项 | 实验目的 | 仪器 |
| A | 除去氯化钠溶液中的泥沙 | 漏斗(带滤纸)、烧杯、玻璃棒 |
| B | 从食盐水中获得NaCl晶体 | 坩埚、玻璃棒、酒精灯、泥三角 |
| C | 用0.10mol•L-1的盐酸测定未知浓度的NaOH溶液浓度 | 碱式滴定管、酸式滴定管、锥形瓶、胶头滴管、烧杯 |
| D | 用MnO2和浓盐酸制取干燥、纯净的Cl2 | 圆底烧瓶、分液漏斗、酒精灯、洗气瓶、集气瓶、导管、石棉网 |
| A. | A | B. | B | C. | C | D. | D |
13.已知有机物A、B之间存在转化关系:A(C6H12O2)+H2O$?_{△}^{稀硫酸}$B+CH3COOH(已配平).则符合条件的B的同分异构体有(不考虑立体异构)( )
0 157701 157709 157715 157719 157725 157727 157731 157737 157739 157745 157751 157755 157757 157761 157767 157769 157775 157779 157781 157785 157787 157791 157793 157795 157796 157797 157799 157800 157801 157803 157805 157809 157811 157815 157817 157821 157827 157829 157835 157839 157841 157845 157851 157857 157859 157865 157869 157871 157877 157881 157887 157895 203614
| A. | 4种 | B. | 5种 | C. | 6种 | D. | 7种 |





 CH3COOC2H5+H2O.
CH3COOC2H5+H2O.