19.如图实验装置或操作不符合实验要求的是( )
| A. |  石油分馏 | B. |  灼烧干海带 | ||
| C. |  用CCl4萃取碘水中的碘 | D. |  治炼金属铁 |
17.埋在地下的输油铸铁管道,在下列各种情况下,被腐蚀速率最慢的是( )
0 157679 157687 157693 157697 157703 157705 157709 157715 157717 157723 157729 157733 157735 157739 157745 157747 157753 157757 157759 157763 157765 157769 157771 157773 157774 157775 157777 157778 157779 157781 157783 157787 157789 157793 157795 157799 157805 157807 157813 157817 157819 157823 157829 157835 157837 157843 157847 157849 157855 157859 157865 157873 203614
| A. | 在含铁元素较多的酸性土壤中 | |
| B. | 在干燥致密不透气的土壤中 | |
| C. | 在潮湿疏松透气的土壤中 | |
| D. | 在含碳粒较多的潮湿透气的中性土壤中 |
 .
.
 .
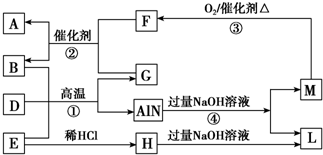
. 金属镁在目前的汽车、航天、航空、机械制造、军事等产业中得到迅猛发展.
金属镁在目前的汽车、航天、航空、机械制造、军事等产业中得到迅猛发展.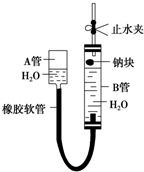 如图是某化学学习小组用来探究钠与水反应的实验装置.该装置可以集反应、收集、检验气体于一体.图中钠块是用大头针叉住的.请填空:
如图是某化学学习小组用来探究钠与水反应的实验装置.该装置可以集反应、收集、检验气体于一体.图中钠块是用大头针叉住的.请填空:
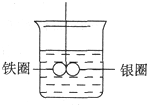 如图所示,在盛有水的烧杯中,铁圈和银圈的连接处吊着一根绝缘的细丝,使之平衡.小心地从烧杯中央滴入CuSO4溶液.
如图所示,在盛有水的烧杯中,铁圈和银圈的连接处吊着一根绝缘的细丝,使之平衡.小心地从烧杯中央滴入CuSO4溶液.