16.下列叙述中正确的是( )
| A. | 化学键只存在于分子之间 | |
| B. | 化学键只存在于离子之间 | |
| C. | 化学键是相邻的原子或离子之间强烈的相互作用 | |
| D. | 化学键是相邻的分子之间强烈的相互作用 |
14.用下列实验装置完成对应的实验(部分仪器已省略),操作正确并能达到实验目的是( )
| A. |  制备氢氧化亚铁 | B. |  石油的分馏 | ||
| C. |  测定盐酸浓度 | D. |  配制稀硫酸 |
13.下列说法正确的是( )
| A. | KW随浓度的改变而改变 | |
| B. | 一般情况下,一元弱酸HA的Ka 越大,表明该酸的酸性越弱 | |
| C. | 对已达到化学平衡的反应,改变压强,平衡常数(K)一定改变 | |
| D. | Ksp只与难溶电解质的性质和温度有关,而与溶液中的离子浓度无关 |
12.在0.1 mol•L-1 CH3COOH溶液中存在如下电离平衡:CH3COOH?CH3COO-+H+,下列叙述正确的是( )
| A. | 加入水时,平衡向逆反应方向移动 | |
| B. | 加入少量NaOH固体,平衡向正反应方向移动 | |
| C. | 加入少量0.1 mol•L-1 HCl溶液,平衡向逆反应方向移动,溶液中c(H+)减小 | |
| D. | 加入少量CH3COONa固体,平衡向正反应方向移动 |
11.下列说法正确的是(NA表示阿伏加德罗常数的数值)( )
| A. | 在常温常压下,11.2 L N2含有的分子数为0.5 NA | |
| B. | 2.4g Mg变为Mg2+时失去的电子数目为0.2NA | |
| C. | 1 L 1mol•L-1 CH3COONa溶液中存在NA个CH3COO- | |
| D. | 1 mol Cn H2n+2含有(3n+2)NA个共价键 |
10.某粒子用${\;}_{Z}^{A}$Rn-表示,下列关于该粒子的叙述正确的是( )
| A. | 所含质子数=Z-n | B. | 所含中子数=A-Z+n | ||
| C. | 质量数=A+n | D. | 所含电子数=Z+n |
9.以下是电化学原理的应用问题.
(1)由A、B、C、D四种金属按下表装置图进行实验.
根据实验现象回答问题:四种金属活动性由强到弱的顺序是D>A>B>C.
(2)氢氧燃料电池是符合绿色化学理念的新型发电装置.如图1为电池示意图,请回答:
①氢氧燃料电池的能量转化的主要形式是由化学能转变为电能,在导线中电子流动方向为由a到b(用a、b表示).
②负极反应式为2H2+4OH--4e-=4H2O(或H2+2OH--2e-=2H2O).
(3)如图2中电极a、b分别为Ag电极和Pt电极,电极c、d都是石墨电极.通电一段时间后,在c、d两极上共收集到336mL(标准状况)气体.回答:
①直流电源中,M为正极.
②AgNO3溶液的浓度(填“增大”“减小”或“不变”.下同)不变,H2SO4溶液的浓度增大.
③此时电路中转移电子的物质的量为0.02mol.
0 157651 157659 157665 157669 157675 157677 157681 157687 157689 157695 157701 157705 157707 157711 157717 157719 157725 157729 157731 157735 157737 157741 157743 157745 157746 157747 157749 157750 157751 157753 157755 157759 157761 157765 157767 157771 157777 157779 157785 157789 157791 157795 157801 157807 157809 157815 157819 157821 157827 157831 157837 157845 203614
(1)由A、B、C、D四种金属按下表装置图进行实验.
| 装置 |  | 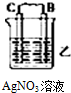 | 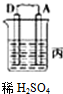 |
| 现象 | 金属A不断溶解 | C极质量增加 | A上有气体产生 |
(2)氢氧燃料电池是符合绿色化学理念的新型发电装置.如图1为电池示意图,请回答:

①氢氧燃料电池的能量转化的主要形式是由化学能转变为电能,在导线中电子流动方向为由a到b(用a、b表示).
②负极反应式为2H2+4OH--4e-=4H2O(或H2+2OH--2e-=2H2O).
(3)如图2中电极a、b分别为Ag电极和Pt电极,电极c、d都是石墨电极.通电一段时间后,在c、d两极上共收集到336mL(标准状况)气体.回答:
①直流电源中,M为正极.
②AgNO3溶液的浓度(填“增大”“减小”或“不变”.下同)不变,H2SO4溶液的浓度增大.
③此时电路中转移电子的物质的量为0.02mol.
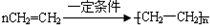 .
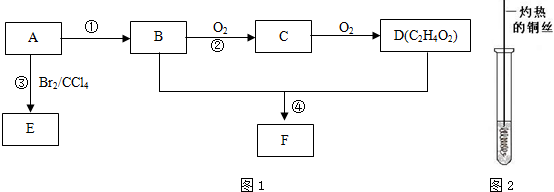
.
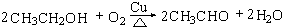 .
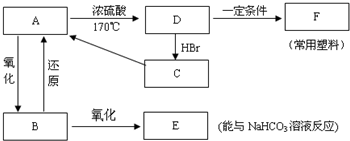
.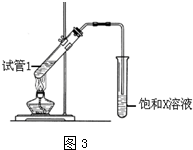 (4)D与碳酸氢钠溶液反应的离子方程式为CH3COOH+HCO3-→CH3COO-+H2O+CO2↑.
(4)D与碳酸氢钠溶液反应的离子方程式为CH3COOH+HCO3-→CH3COO-+H2O+CO2↑.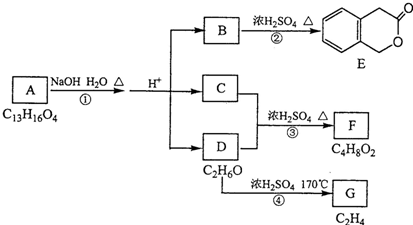
 .反应①的反应类型是水解反应或取代反应.
.反应①的反应类型是水解反应或取代反应. .
. .
.