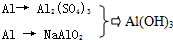4.X、Y、Z、M为原子序数依次增大的4种短周期元素.已知X、Y、Z是同周期的相邻元素,M原子的核外电子数是Z原子最外层电子数的2倍,Y与其同主族的短周期元素可形成一种常见的气体.下列说法正确的是( )
| A. | 原子半径:M>Y | B. | 对应氢化物的沸点:M>Z | ||
| C. | 对应氢化物的稳定性:X>Y | D. | XY2与MY2溶于水都能得到对应的酸 |
3.下列说法正确的是( )
| A. | 实验室制备Cl2,可用排饱和食盐水集气法收集 | |
| B. | 浓盐酸与KMnO4制氯气的离子方程式是:MnO4-+8H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+4H2O | |
| C. | 漂白粉溶液在空气中失效变化的离子方程式是:ClO-+CO2+H2O=HClO+HCO3- | |
| D. | H2O2具有很强的氧化性,在化学反应中只能作氧化剂 |
2.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,5.6 L CO2与足量Na2O2反应转移的电子数为0.5 NA | |
| B. | 78 g苯含有碳碳双键的数目为3 NA | |
| C. | 常温下,4.4gCO2和N2O混合物中所含有的原子数为0.3 NA | |
| D. | 1 L 1 mol•L-1的CuSO4溶液中含NA个Cu2+ |
1.由A、B、C、D四种金属按下表中装置图进行实验.
根据实验现象回答下列问题:
(1)装置甲中负极的电极反应式是A-2e-═A2+.
(2)装置乙中正极的电极反应式是Cu2++2e-═Cu.
(3)四种金属活泼性由强到弱的顺序是D>A>B>C.
(4)A、C形成合金,露置在潮湿空气中,A先被腐蚀.
| 装置 | 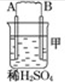 | 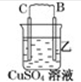 | 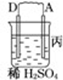 |
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
(1)装置甲中负极的电极反应式是A-2e-═A2+.
(2)装置乙中正极的电极反应式是Cu2++2e-═Cu.
(3)四种金属活泼性由强到弱的顺序是D>A>B>C.
(4)A、C形成合金,露置在潮湿空气中,A先被腐蚀.
20.下列相关实验或现象的描述正确的是( )
| A. | 甲烷中混有的乙烯,可以用酸性KMnO4溶液洗气除去 | |
| B. | 乙烯、苯都易燃烧,燃烧时都产生明亮火焰、大量黑烟 | |
| C. | 乙酸乙酯、油脂都能水解,且在热的NaOH溶液中水解更完全 | |
| D. | 葡萄糖、淀粉都有还原性,都能与新制Cu(OH)2共热产生砖红色沉淀 |
19.下列化学用语正确的是( )
| A. | 氟离子的结构示意图: | B. | 氨分子的电子式: | ||
| C. | 丙烯的结构简式:CH3CHCH2 | D. | 乙烯的球棍模型: |
18.下列关于元素周期表的叙述正确的是( )
| A. | 元素周期表中有七行,七个周期,有18列,18个族 | |
| B. | 目前使用的元素周期表中,同一主族的元素最外层电子数相同 | |
| C. | 短周期元素是指1~20号元素,其中大多数为非金属 | |
| D. | 元素周期表中,元素的种数与对应的原子种数一样多 |
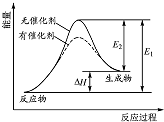
17.某化学反应过程的能量变化如图所示.下列说法正确的是( )
0 157650 157658 157664 157668 157674 157676 157680 157686 157688 157694 157700 157704 157706 157710 157716 157718 157724 157728 157730 157734 157736 157740 157742 157744 157745 157746 157748 157749 157750 157752 157754 157758 157760 157764 157766 157770 157776 157778 157784 157788 157790 157794 157800 157806 157808 157814 157818 157820 157826 157830 157836 157844 203614

| A. | 该反应的反应物总能量高于生成物总能量 | |
| B. | 使用催化剂可以增大该反应的反应热 | |
| C. | 该化学反应的反应热为E1,且反应放热 | |
| D. | 化学反应在物质变化的同时,必然伴随能量变化 |
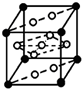 已知A、B、C、D、E、F是元素周期表中前36号元素,它们的原子序数依次增大.A的质子数、电子层数、最外层电子数均相等,B元素基态原子中电子占据三种能量不同的原子轨道且每种轨道中的电子总数相同,D的基态原子核外成对电子数是成单电子数的3倍,E是第四周期d区原子序数最大的元素,F+的最外层电子排布全充满.请回答下列问题:
已知A、B、C、D、E、F是元素周期表中前36号元素,它们的原子序数依次增大.A的质子数、电子层数、最外层电子数均相等,B元素基态原子中电子占据三种能量不同的原子轨道且每种轨道中的电子总数相同,D的基态原子核外成对电子数是成单电子数的3倍,E是第四周期d区原子序数最大的元素,F+的最外层电子排布全充满.请回答下列问题: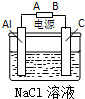 甲、乙、丙三位同学按下列方法制取氢氧化铝,请你参与并回答有关问题.
甲、乙、丙三位同学按下列方法制取氢氧化铝,请你参与并回答有关问题.